
Wetenschap
Ionische geleidbaarheid van NaCl:vaste versus gesmolten toestand uitgelegd
1. Ionische aard van NaCl:
* Natriumchloride (NaCl) is een ionische verbinding. Dit betekent dat het wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
2. Vaste toestand:
* In vaste toestand zijn deze ionen opgesloten in een stijf, kristallijn rooster. De ionen zijn stevig verpakt en op hun plaats gehouden door sterke elektrostatische krachten. Deze stijve structuur verhindert de vrije beweging van ionen.
* Zonder vrij bewegende ladingsdragers (zoals ionen) kan elektriciteit niet stromen. Daarom is vast NaCl een slechte geleider van elektriciteit.
3. Gesmolten staat:
* Wanneer NaCl smelt, breken de ionen los van hun vaste posities. De sterke elektrostatische krachten die de ionen bij elkaar houden, worden zwakker, waardoor ze vrijer kunnen bewegen.
* Deze mobiele ionen fungeren als ladingsdragers. Wanneer een spanning wordt aangelegd, bewegen de positieve natriumionen naar de negatieve elektrode, en de negatieve chloride-ionen naar de positieve elektrode. Deze ionenstroom vormt een elektrische stroom.
Samengevat:
* Vast NaCl: Ionen zijn gefixeerd, geen vrije ladingsdragers, geen geleidbaarheid.
* Gesmolten NaCl: Ionen zijn mobiel, gratis ladingsdragers, goede geleiding.
Hoofdlijnen
- Wat zijn de basisvaardigheden in de wetenschap?
- Plaatsen waar cellen watervoedsel en andere materialen opslaan?
- Celbioloog legt uit hoe RNA-virussen zichzelf kopiëren
- Wat is het specifieke proces waarmee cel zijn DNA kopieert?
- Hoe worden cellen genoemd als ze samen groeperen?
- Hoe helpt evolutie wetenschappers?
- Planktivoren:wat ze eten en hun rol in het ecosysteem
- Wat zijn vier soorten immuniteit?
- Schimmeluitbraak bedreigt driekleurige vleermuis met uitsterven
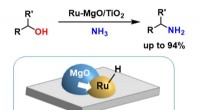
- Een verbeterde op ruthenium gebaseerde katalysator voor de synthese van primaire amines
- Een kwestie van mobiliteit:multidisciplinair artikel suggereert nieuwe strategie voor medicijnontdekking
- OLED's worden helderder en duurzamer

- Praktische wetenschappelijke activiteiten om bevroren vloeistoffen te onderzoeken

- Een stap dichter bij ontwerp-on-demand steigers voor weefselregeneratie

 Wat zijn de afbranden van windenergie?
Wat zijn de afbranden van windenergie?  Wat is de zwaartekracht van Google?
Wat is de zwaartekracht van Google?  Wat maakt dat een vetzuur meer ATP produceert?
Wat maakt dat een vetzuur meer ATP produceert?  Exotische koolstofmicrokristallen in meteorietstof
Exotische koolstofmicrokristallen in meteorietstof Hoe de integriteit van enquêteonderzoek te beschermen:12 aanbevelingen
Hoe de integriteit van enquêteonderzoek te beschermen:12 aanbevelingen  Welke van de Suns -lagen is alleen zichtbaar tijdens eclipsen?
Welke van de Suns -lagen is alleen zichtbaar tijdens eclipsen?  Wat is nodig voor de productie van kernenergie?
Wat is nodig voor de productie van kernenergie?  Hernieuwbare en niet-hernieuwbare bronnen voor kinderen
Hernieuwbare en niet-hernieuwbare bronnen voor kinderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


