
Wetenschap
HCl versus CH3COOH:ionisatiegraden begrijpen - chemie uitgelegd
HCl (Zoutzuur)
* Sterk zuur: HCl is een sterk zuur, wat betekent dat het in water vrijwel volledig ioniseert.
* Hoge mate van ionisatie: In oplossing doneert HCl zijn proton (H+) gemakkelijk aan water, waardoor H3 ontstaat O+ (hydroniumion) en Cl- (chloride-ion). Het evenwicht ligt sterk in de richting van de geïoniseerde vorm.
* In wezen 100% geïoniseerd: We beschouwen HCl doorgaans als 100% geïoniseerd in verdunde waterige oplossingen.
CH3 COOH (azijnzuur)
* Zwak zuur: Azijnzuur is een zwak zuur, wat betekent dat het slechts gedeeltelijk in water ioniseert.
* Lage mate van ionisatie: Slechts een klein deel van de azijnzuurmoleculen doneert hun proton aan water en vormt H3 O+ en CH3 COO- (acetaation). Het evenwicht is in het voordeel van de niet-geïoniseerde vorm.
* Beperkte ionisatie: Azijnzuur bereikt een evenwicht waarbij een klein maar significant deel in zijn moleculaire vorm blijft.
Belangrijkste verschillen
* Kracht: HCl is een sterk zuur, terwijl CH3 COOH is een zwak zuur.
* Ionisatiepercentage: HCl ioniseert bijna volledig (bijna 100%), terwijl CH3 COOH ioniseert slechts gedeeltelijk.
* Evenwicht: Het evenwicht voor HCl ligt sterk in de richting van de geïoniseerde vorm, terwijl het evenwicht voor CH3 COOH is voorstander van de niet-geïoniseerde vorm.
Samengevat:
HCl heeft een veel hogere ionisatiegraad dan CH3 COOH vanwege zijn aard als een sterk zuur. Dit betekent dat een oplossing van HCl aanzienlijk meer H+-ionen zal bevatten dan een oplossing van azijnzuur bij dezelfde concentratie.
 Unieke organische lichtemitterende moleculaire emitters
Unieke organische lichtemitterende moleculaire emitters Welke chemische cyclus gebruikt bacteriën om gassen uit de lucht te repareren?
Welke chemische cyclus gebruikt bacteriën om gassen uit de lucht te repareren?  Is het ontladen van een batterij een chemische verandering?
Is het ontladen van een batterij een chemische verandering?  Wat gebeurt er als een stikstofatoom opgewonden wordt van het passeren van elektron?
Wat gebeurt er als een stikstofatoom opgewonden wordt van het passeren van elektron?  Chemici gebruiken kunstmatige intelligentie om de toekomst (van chemische reacties) te voorspellen
Chemici gebruiken kunstmatige intelligentie om de toekomst (van chemische reacties) te voorspellen
 Herbebossing in stedelijke landschappen
Herbebossing in stedelijke landschappen Omgaan met verkiezingsangst? De psychiater legt uit hoe je je angsten kunt kanaliseren en het tribale denken kunt doorbreken
Omgaan met verkiezingsangst? De psychiater legt uit hoe je je angsten kunt kanaliseren en het tribale denken kunt doorbreken  Helpen dierentuinprogramma's bedreigde diersoorten te redden?
Helpen dierentuinprogramma's bedreigde diersoorten te redden?  Verafschuwd door wetenschappers, geliefd door de natuur:Zwavel en de oorsprong van het leven
Verafschuwd door wetenschappers, geliefd door de natuur:Zwavel en de oorsprong van het leven  Van fossielen tot brandstof:energiepotentieel van het Maniamba-bekken in Mozambique
Van fossielen tot brandstof:energiepotentieel van het Maniamba-bekken in Mozambique
Hoofdlijnen
- Hoe noem je een organisme dat ziekten of plasmidenvirussen draagt, bacteriën?
- Wat is een kenmerk van wei-eiwit?
- Wat is forensische genetische genealogie? De techniek die in de zaak Rachel Morin werd gebruikt, is nauwelijks gereguleerd
- Tropische regenwouden tonen de fosforsleutel om de ecosystemen van de wereld te begrijpen
- Uit onderzoek blijkt dat er bij het ouder worden een aparte populatie van onruststokende bloedplaatjescellen verschijnt
- Welk systeem in het lichaam bevat informatie van klieren en organen tot hersenen?
- Welk deel van een plant is het meest zijn voedsel geproduceerd?
- Wat is Quantum-Noetics?
- Voordat de celdeling begint, bestaat elke chromosomen uit twee identieke verbonden genaamd?
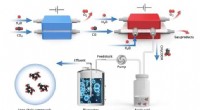
- Hybride elektro-biosysteem upcyclet koolstofdioxide tot energierijke verbindingen met lange ketens
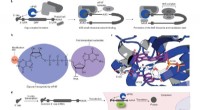
- Nieuwe inzichten in processen op moleculair niveau kunnen corrosie helpen voorkomen en de katalytische conversie verbeteren

- Elektriciteit gebruiken om de hoeveelheid gegevens te vergroten die door DNA kan worden opgeslagen

- Biochemici gebruiken nieuwe tool om mRNA te controleren door middel van licht
- Spontaan patronen creëren in synthetische materialen

 Koolstof 13 wat wordt het na verval?
Koolstof 13 wat wordt het na verval?  Wat zat er achter het aardappeltekort in Australië? Nat weer en moeilijk te beheersen ziekten
Wat zat er achter het aardappeltekort in Australië? Nat weer en moeilijk te beheersen ziekten  Hoeveel water is nodig om zout op te lossen?
Hoeveel water is nodig om zout op te lossen?  Schaalbare fotonische computer lost het deelverzamelingsomprobleem op
Schaalbare fotonische computer lost het deelverzamelingsomprobleem op Metaalhoudende verbindingen zijn veelbelovend als HIV-wapen
Metaalhoudende verbindingen zijn veelbelovend als HIV-wapen  Wat is de energietransformatie tijdens de werking van een zonne -calculator?
Wat is de energietransformatie tijdens de werking van een zonne -calculator?  Wat zal een verandering in de hoeveelheid waterdamp in de atmosfeer veroorzaken?
Wat zal een verandering in de hoeveelheid waterdamp in de atmosfeer veroorzaken?  Veranderende atmosferische omstandigheden kunnen bijdragen aan sterkere oceaangolven op Antarctica
Veranderende atmosferische omstandigheden kunnen bijdragen aan sterkere oceaangolven op Antarctica
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

