
Wetenschap
Bepaling van de empirische formule van een koolstofrijke koolwaterstof
1. Ga uit van een monster van 100 g
* Dit maakt de berekeningen eenvoudiger, omdat de percentages direct naar grammen worden vertaald.
* Je hebt 85,7 g koolstof en (100 - 85,7) =14,3 g waterstof.
2. Converteer gram naar mol
* Gebruik de molaire massa van elk element:
* Koolstof (C):12,01 g/mol
* Waterstof (H):1,01 g/mol
* Mol koolstof:85,7 g / 12,01 g/mol =7,14 mol
* Mol waterstof:14,3 g / 1,01 g/mol =14,2 mol
3. Vind de eenvoudigste molverhouding
* Deel elk aantal mol door het kleinste aantal mol (in dit geval 7,14):
* Koolstof:7,14 mol / 7,14 mol =1
* Waterstof:14,2 mol / 7,14 mol =2
4. Schrijf de empirische formule
* De empirische formule vertegenwoordigt de eenvoudigste gehele getalsverhouding van atomen in de verbinding.
* De empirische formule voor deze koolwaterstof is CH₂ .
 Netwerkvaste stoffen:covalente bindingsstructuren begrijpen
Netwerkvaste stoffen:covalente bindingsstructuren begrijpen  HCl en waterreactie:moleculaire vergelijking en uitleg
HCl en waterreactie:moleculaire vergelijking en uitleg  De vingerafdrukken van moleculen berekenen met kunstmatige intelligentie
De vingerafdrukken van moleculen berekenen met kunstmatige intelligentie pH-schaal uitgelegd:zuurgraad en waterstofionen begrijpen
pH-schaal uitgelegd:zuurgraad en waterstofionen begrijpen  Wat resulteert de overdracht van elektronen van natriumatomen naar chloor in de vorming van?
Wat resulteert de overdracht van elektronen van natriumatomen naar chloor in de vorming van?
 Een bos dat meestal evelgreens bevat?
Een bos dat meestal evelgreens bevat?  Ozark graslanden ervaren grote toename van bomen en struiken
Ozark graslanden ervaren grote toename van bomen en struiken Waar in de natuur komen staande golven voor?
Waar in de natuur komen staande golven voor?  Hoeveel stroom verbruikt de wereld?
Hoeveel stroom verbruikt de wereld?  Wereldwijd oceaanrapport toont ongekende impact van klimaatverandering, aangezien de Noordpoolregisters lage ijsniveaus registreren
Wereldwijd oceaanrapport toont ongekende impact van klimaatverandering, aangezien de Noordpoolregisters lage ijsniveaus registreren
Hoofdlijnen
- Wat is een verzameling voor pus in de lichaamsholte?
- Een 'zenuwstelsel' voor mierenkolonies? Kolonie reageert op predatiesimulatie als een 'superorganisme'
- In welk type organismen komt fotosynthese op?
- Waarom is ribosoom belangrijk voor de cel?
- Waarom moet je je lus niet vlammen en er dan snel bacteriën mee proberen op te pikken?
- Wat is de functie van cuticula?
- Onderzoek toont aan hoe externe ecologische gemeenschappen de co-evolutie van gastheren en hun parasieten kunnen beïnvloeden
- Hoe duurzaam is tonijn? Nieuwe mondiale vangstdatabank legt gevaarlijke visserijtrends bloot
- Welk biome heeft eekhoorns muizen konijnen en herten?
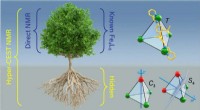
- Hyper-CEST NMR-techniek onthult ontbrekende structuur van een nieuw containermolecuul
- Hoe u de pH van water veilig en effectief kunt verlagen voor aquaria

- Pig-Pen-effect:het mengen van huidolie en ozon kan een persoonlijke vervuilingswolk veroorzaken
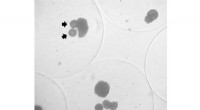
- Kleine medicijnafgiftecapsules kunnen getransplanteerde insulineproducerende cellen ondersteunen
- Ammoniumnitraat en jodium:een terugblik op de explosieve geschiedenis van twee essentiële stoffen

 Hoe is verwering gerelateerd aan de geologische cyclus?
Hoe is verwering gerelateerd aan de geologische cyclus?  Wat is het proces waarin lagen rotsschilfer een grotere verwering van een groter vlokken?
Wat is het proces waarin lagen rotsschilfer een grotere verwering van een groter vlokken?  Is de volgende zin waar of onwaar gefaciliteerde diffusie, hoeft geen energie te gebruiken?
Is de volgende zin waar of onwaar gefaciliteerde diffusie, hoeft geen energie te gebruiken?  Wat zijn niet-de-ziekte-producerende micro-organismen?
Wat zijn niet-de-ziekte-producerende micro-organismen?  Wat is de energie in een veerbalkapparaat voordat deze werd vrijgegeven?
Wat is de energie in een veerbalkapparaat voordat deze werd vrijgegeven?  Onbekende helpers van de bodem:hoe ongewervelde dieren afbraakplanten ondersteunen
Onbekende helpers van de bodem:hoe ongewervelde dieren afbraakplanten ondersteunen  Hoe moeten scheidsrechters technologie gebruiken in het voetbal?
Hoe moeten scheidsrechters technologie gebruiken in het voetbal?  Hoe heet bacteriën?
Hoe heet bacteriën?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

