
Wetenschap
Fluorbinding:covalent versus ionisch - Chemische bindingen begrijpen
* Elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen.
* Ionisatie-energie: Hoewel fluor een elektron kan opnemen, is de ionisatie-energie (de energie die nodig is om een elektron te verwijderen) erg hoog. Dit betekent dat het moeilijk is om het een elektron te laten verliezen en een positief ion te laten vormen.
* Verbindingsneiging: Vanwege zijn hoge elektronegativiteit en hoge ionisatie-energie geeft fluor er de voorkeur aan elektronen te delen met andere atomen in plaats van ze volledig te verwerven of te verliezen.
Er zijn echter enkele uitzonderingen:
* Met alkalimetalen en aardalkalimetalen: Fluor kan ionische bindingen vormen met deze zeer elektropositieve elementen. Het grote verschil in elektronegativiteit leidt tot de volledige overdracht van elektronen, waardoor ionen als NaF (natriumfluoride) en CaF₂ (calciumfluoride) ontstaan.
Samenvattend vormt fluor voornamelijk covalente bindingen vanwege de hoge elektronegativiteit ervan en de moeilijkheid om de elektronen te verwijderen. Het kan echter ionische bindingen vormen met zeer elektropositieve elementen.
 Wat is het symbool van een arseen -ion?
Wat is het symbool van een arseen -ion?  Waarom is het onjuist om over smeltpunt te spreken?
Waarom is het onjuist om over smeltpunt te spreken?  Wie heeft een hogere elektronenaffiniteit tussen broom en jodium?
Wie heeft een hogere elektronenaffiniteit tussen broom en jodium?  Welke belangrijke ontwikkelingen vonden plaats in wetenschappelijke instrumenten?
Welke belangrijke ontwikkelingen vonden plaats in wetenschappelijke instrumenten?  Hoe zou je een stripverhaal maken waarin suiker verandert van vast naar vloeibaar?
Hoe zou je een stripverhaal maken waarin suiker verandert van vast naar vloeibaar?
 Klimaatverandering veroorzaakt een dramatische daling van de biodiversiteit en het visserijpotentieel van de Perzische Golf
Klimaatverandering veroorzaakt een dramatische daling van de biodiversiteit en het visserijpotentieel van de Perzische Golf Opwarming van de aarde tegengaan door CO2-opslag? Controleer op continentale stress
Opwarming van de aarde tegengaan door CO2-opslag? Controleer op continentale stress Difference Between Community & Ecosystem
Difference Between Community & Ecosystem Extreem gevaarlijke orkaan Eta treft Nicaragua
Extreem gevaarlijke orkaan Eta treft Nicaragua Enorme bosbranden in het westen van de VS brengen nevel naar de oostkust
Enorme bosbranden in het westen van de VS brengen nevel naar de oostkust
Hoofdlijnen
- Wat is de stabiele interne omgeving van cellen?
- Wat produceren de C -cellen van schildklier?
- Zeegrasweiden breiden zich snel uit nabij bewoonde eilanden op de Malediven
- Vier wetenschappelijke manieren om te zien of je kat van je houdt
- Wat zijn de twee fasen van de menselijke evolutie?
- Evolutie ontmoet biochemie om beter te begrijpen hoe dopamine-receptoren werken
- Wat is animally -protist pseudopoden?
- Satellietvolging geeft aanwijzingen over verloren jaren aan Zuid-Atlantische zeeschildpadden
- Welke van deze termen zou niet worden geassocieerd met DNA tijdens mitose?
- Niet zo snel:sommige batterijen kunnen te ver worden geduwd
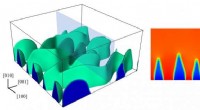
- Onderzoekers ontdekken hoe een eiwit de nadelige gevolgen van waterverlies in cellen vermindert

- Wetenschappers stellen een flexibel interface-ontwerp voor een silicium-grafiet dual-ion batterij voor
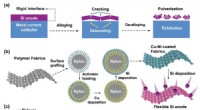
- Onderzoekers stellen nieuwe strategie voor om methaanhydroxylering te verbeteren
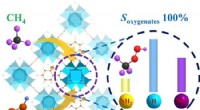
- Nieuwe zouten leggen de lat hoger voor lithium-ionbatterijtechnologie

 Wat is een groep organismen gevonden in stabiele opvolging van het podium?
Wat is een groep organismen gevonden in stabiele opvolging van het podium?  Welke richting reist elektromagnetische golven?
Welke richting reist elektromagnetische golven?  Een strategische onderzoeksagenda om land en bodem in Europa beter te benutten
Een strategische onderzoeksagenda om land en bodem in Europa beter te benutten De planeten in het zonnestelsel draaien rond de zon omdat het de grootste en sterkste aantrekkingskracht heeft?
De planeten in het zonnestelsel draaien rond de zon omdat het de grootste en sterkste aantrekkingskracht heeft?  Elementen wiens atomen kunnen combineren om verbindingen te vormen?
Elementen wiens atomen kunnen combineren om verbindingen te vormen?  Wat is de evolutietheorie en wie heeft het gezegd?
Wat is de evolutietheorie en wie heeft het gezegd?  Meren verbinden met het oog op de toekomst
Meren verbinden met het oog op de toekomst Inheemse verdedigers staan tussen illegale wegen en het voortbestaan van het Amazone-regenwoud
Inheemse verdedigers staan tussen illegale wegen en het voortbestaan van het Amazone-regenwoud
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

