
Wetenschap
Sterkte van organische zuren:inzicht in de impact van chloorvervanging
Kracht van organische zuren versus chloor-gesubstitueerde zuren
Algemene trend: Met chloor gesubstitueerde zuren zijn sterker dan hun ongesubstitueerde tegenhangers.
Uitleg:
* Inductief effect: Chloor is elektronegatiever dan koolstof. Dit betekent dat het de elektronendichtheid naar zich toe trekt, waardoor een gedeeltelijke positieve lading ontstaat op het aangrenzende koolstofatoom. Dit 'elektronenzuigende' effect staat bekend als het inductieve effect stabiliseert de geconjugeerde base van het zuur door de negatieve lading te verspreiden.
* Stabilisatie van geconjugeerde base: Hoe stabieler de geconjugeerde base, hoe sterker het zuur. Omdat de geconjugeerde base van een chloor-gesubstitueerd zuur wordt gestabiliseerd door het inductieve effect van chloor, is deze zwakker en daarom is het zuur sterker.
Voorbeeld:
* Azijnzuur (CH3COOH) is een zwakker zuur dan chloorazijnzuur (ClCH2COOH) .
* Propionzuur (CH3CH2COOH) is een zwakker zuur dan 3-chloorpropionzuur (ClCH2CH2COOH) .
Factoren die de kracht beïnvloeden:
* Aantal chlooratomen: Hoe meer chlooratomen aanwezig zijn, hoe sterker de inductieve werking en hoe sterker het zuur.
* Positie van chlooratoom: Chlooratomen dichter bij de carboxylgroep hebben een groter inductief effect.
Uitzonderingen:
* Sterisch effect: In sommige gevallen kan de sterische hinder veroorzaakt door meerdere chlooratomen de nadering van de base belemmeren, wat leidt tot een afname van de zuurgraad.
Samengevat:
Met chloor gesubstitueerde zuren zijn over het algemeen sterker dan ongesubstitueerde organische zuren vanwege het stabiliserende inductieve effect van chlooratomen. Hoe meer chlooratomen aanwezig zijn en hoe dichter ze bij de carboxylgroep zijn, hoe sterker het zuur. In bepaalde gevallen kunnen sterische effecten echter een rol spelen.
 Wat is de IUPAC -naam van een benzeenring die aan een ander als substituent is geactiveerd?
Wat is de IUPAC -naam van een benzeenring die aan een ander als substituent is geactiveerd?  Waterstofproductiemethoden:waterstof scheiden van lucht - een uitgebreide gids
Waterstofproductiemethoden:waterstof scheiden van lucht - een uitgebreide gids  Nieuw onderzoek toont aan dat alle solid-state batterijen met de hoogste energiedichtheid nu mogelijk zijn
Nieuw onderzoek toont aan dat alle solid-state batterijen met de hoogste energiedichtheid nu mogelijk zijn Waarom vormen de elementen natrium- en kalium -ionen met dezelfde lading?
Waarom vormen de elementen natrium- en kalium -ionen met dezelfde lading?  Inzicht in anionen gevormd bij ionische binding:een uitgebreide gids
Inzicht in anionen gevormd bij ionische binding:een uitgebreide gids
 Hoe kan Euglena zich ontdoen van afval?
Hoe kan Euglena zich ontdoen van afval?  De vulkaan van Hawaï zou zich kunnen ontwikkelen tot een grote uitbarsting:wetenschappers
De vulkaan van Hawaï zou zich kunnen ontwikkelen tot een grote uitbarsting:wetenschappers Hoe beïnvloeden bomen het weer?
Hoe beïnvloeden bomen het weer?  Fossiele motten laten hun ware aard zien
Fossiele motten laten hun ware aard zien  Wat klimaatactivisten kunnen leren van First Nations-campagnes tegen de fossiele brandstofindustrie
Wat klimaatactivisten kunnen leren van First Nations-campagnes tegen de fossiele brandstofindustrie
Hoofdlijnen
- Wat groeit sneller dan een cel die het dwingt om te delen?
- Welke organel laat chemicaliën vrij die cellen van organellen afbreken en recyclen?
- Dit wetenschappelijke experiment duurt 500 jaar
- Als je Botany bestudeert, waar leer dan over?
- Nieuw soort cognitieve robot... een puppy?
- Wat is je kont echt op wetenschappelijke manier genoemd?
- In zaadplanten wordt de structuur die de mannelijke gametofyt omsluit en naar een andere plant transporteert een?
- Welke observatie bewijst dat een cel eukaryote is?
- Thuis op het strand:Antelope krijgt nieuwe opgravingen in New Orleans
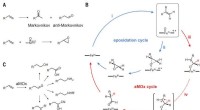
- Gemodificeerd enzym dat wordt gebruikt voor een betere anti-Markovnikov-selectiviteit bij alkeenoxidaties
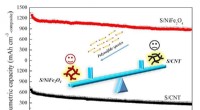
- Nikkelferriet bevordert de capaciteit en cyclusstabiliteit van lithium-zwavelbatterijen
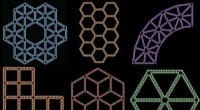
- Computerprogramma kan een 2D-tekening in vrije vorm vertalen naar een DNA-structuur
- Carbon black gerecycled uit autobanden

- Natuurkundigen maken stop-actiebeelden van door licht aangestuurde moleculaire reactie

 Het kosmische waterpad ontdekt door Herschel
Het kosmische waterpad ontdekt door Herschel Wat betekent fysieke eigenschappen in wetenschapstermen?
Wat betekent fysieke eigenschappen in wetenschapstermen?  Een kenmerk van mutaties is dat ze meestal?
Een kenmerk van mutaties is dat ze meestal?  Hoe u het hart van uw hond gezond kunt houden
Hoe u het hart van uw hond gezond kunt houden Nieuwe technologie maakt metalen draden op zonnecellen bijna onzichtbaar voor licht
Nieuwe technologie maakt metalen draden op zonnecellen bijna onzichtbaar voor licht Is een speciaal type eiwit dat alle chemie regelt?
Is een speciaal type eiwit dat alle chemie regelt?  Hoe is Andromeda een sterrenbeeld geworden?
Hoe is Andromeda een sterrenbeeld geworden?  Wat is het antoniem van de natuurkunde?
Wat is het antoniem van de natuurkunde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

