
Wetenschap
Waterstofhalidetests:identificatie en reacties
Tests voor waterstofhalogeniden:
1. Lakmoespapiertest:
* Zuurachtige aard: Waterstofhalogeniden zijn zuur van aard. Ze kleuren blauw lakmoespapier rood, wat wijst op de aanwezigheid van H+-ionen.
2. Zilvernitraattest:
* Vorming van neerslag: Toevoeging van zilvernitraat (AgNO3)-oplossing aan een waterstofhalogenide-oplossing resulteert in de vorming van een neerslag, dat een zilverhalogenide (AgX) is.
* AgCl (zilverchloride): Wit neerslag, onoplosbaar in verdund salpeterzuur.
* AgBr (zilverbromide): Crèmekleurig neerslag, enigszins oplosbaar in verdund salpeterzuur.
* AgI (zilverjodide): Geel neerslag, vrijwel onoplosbaar in verdund salpeterzuur.
* Opmerking: Deze test is nuttig om onderscheid te maken tussen verschillende halogeniden.
3. Reactie met metaaloxiden:
* Vorming van zout en water: Waterstofhalogeniden reageren met metaaloxiden en vormen een zout en water.
* Voorbeeld:
* 2HCl + CuO → CuCl2 + H2O
4. Reactie met metalen:
* Vorming van zout en waterstofgas: Waterstofhalogeniden reageren met actieve metalen om een zout te vormen en waterstofgas vrij te maken.
* Voorbeeld:
* 2HCl + Zn → ZnCl2 + H2
5. Reactie met basen:
* Neutralisatie: Waterstofhalogeniden reageren met basen en vormen zout en water.
* Voorbeeld:
* HCl + NaOH → NaCl + H2O
6. Oxidatiemiddelen:
* Oxidatie tot halogenen: Sterke oxidatiemiddelen, zoals kaliumpermanganaat (KMnO4) of kaliumdichromaat (K2Cr2O7) in zuur medium, kunnen waterstofhalogeniden oxideren tot hun respectievelijke halogenen.
* Voorbeeld:
* 2HCl + KMnO4 + H2SO4 → Cl2 + MnSO4 + K2SO4 + H2O
7. Fysieke eigenschappen:
* Rokend: Waterstofhalogeniden (behalve HF) zijn rokende gassen vanwege hun hoge reactiviteit met vocht in de lucht.
* Oplosbaarheid: Waterstofhalogeniden zijn zeer oplosbaar in water.
8. Specifieke tests voor individuele halogeniden:
* HF: Etst glas door de vorming van hexafluorsilicaationen.
* HCl: Vormt witte dampen van ammoniumchloride (NH4Cl) bij blootstelling aan ammoniak.
* HBr: Ontkleurt broomwater vanwege zijn reducerende eigenschappen.
* Hallo: Ontkleurt kaliumpermanganaatoplossing vanwege de sterk reducerende eigenschappen.
Deze tests kunnen afzonderlijk of in combinatie worden gebruikt om de aanwezigheid van waterstofhalogeniden te identificeren en onderscheid te maken tussen verschillende halogeniden.
 Welk paar elementen heeft de meest vergelijkbare chemische eigenschappen?
Welk paar elementen heeft de meest vergelijkbare chemische eigenschappen?  Hoe worden de niet-natuurlijke elementen van het periodieke tabel genoemd?
Hoe worden de niet-natuurlijke elementen van het periodieke tabel genoemd?  Welk type binding is waarschijnlijk betrokken bij de monsters die in hun pure vorm geen geleiders waren, maar een stroom geleidden wanneer ze zich vermengden met water?
Welk type binding is waarschijnlijk betrokken bij de monsters die in hun pure vorm geen geleiders waren, maar een stroom geleidden wanneer ze zich vermengden met water?  Wanneer een fysieke veranderingen plaatsvinden, worden nieuwe stof gevormd?
Wanneer een fysieke veranderingen plaatsvinden, worden nieuwe stof gevormd?  Wat is de formule voor de combinatie van calcium en stikstof?
Wat is de formule voor de combinatie van calcium en stikstof?
 De beschikbaarheid van water is veranderd, en de mens is de schuldige
De beschikbaarheid van water is veranderd, en de mens is de schuldige Meer EV's kunnen de CO2-uitstoot in Hawaï in minder dan 30 jaar met 93% verminderen
Meer EV's kunnen de CO2-uitstoot in Hawaï in minder dan 30 jaar met 93% verminderen Hoe beïnvloeden landvormen en wateren het klimaat?
Hoe beïnvloeden landvormen en wateren het klimaat?  Verwacht een bovengemiddeld Atlantisch orkaanseizoen, Amerikaanse voorspellers zeggen:
Verwacht een bovengemiddeld Atlantisch orkaanseizoen, Amerikaanse voorspellers zeggen: Ontdekking van Oost-Aziatische moessondynamiek
Ontdekking van Oost-Aziatische moessondynamiek
Hoofdlijnen
- Schapen kunnen menselijke gezichten van foto's herkennen
- Wat is het structurele en functie -kenmerk van diafyse?
- Kloneringsonderzoek begrijpen:soorten, toepassingen en ethische overwegingen
- Wat is het mannelijke deel van de plant dat pollen produceert die wordt genoemd?
- Welke bescherming van het sperma tegen bacteriën is de functie?
- Wat is bacteriële suspensie?
- Wat is het gevoelige deel van een smaakcel?
- Welke twee wetenschapper ontdekte deeltjes die de kern vormen?
- Hoeveel chromosomen zijn er in cellen van het menselijk lichaam?
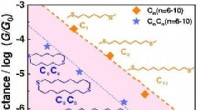
- Zeer isolerende alkaanringen met destructieve σ-interferentie
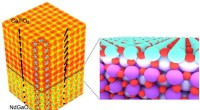
- Een kristallisatiekamer ontwerpen

- Wetenschappers vinden goedkopere manier om waterstof uit water te maken

- Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen
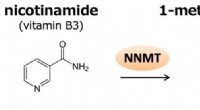
- Pilaarachtige moleculen als biosensoren voor metabolieten
 Welk jaar gaf Regulus licht af als je vandaag naar de ster kijkt?
Welk jaar gaf Regulus licht af als je vandaag naar de ster kijkt?  Wat is een voordeel van meercellig organisme?
Wat is een voordeel van meercellig organisme?  Tsunamiwacht voor Hawaï opgeheven na aardbeving in het noorden van de Stille Oceaan
Tsunamiwacht voor Hawaï opgeheven na aardbeving in het noorden van de Stille Oceaan Wat is het hoofdkation buiten cellen?
Wat is het hoofdkation buiten cellen?  Een fenotypische verhouding van 9331 is kenmerkend voor wat?
Een fenotypische verhouding van 9331 is kenmerkend voor wat?  Wat beschrijft het beste hoe eiwit zich vormt?
Wat beschrijft het beste hoe eiwit zich vormt?  Een beter biosensorpolymeer bouwen
Een beter biosensorpolymeer bouwen Waarom zijn durfkapitalisten zo oprichtersvriendelijk geworden?
Waarom zijn durfkapitalisten zo oprichtersvriendelijk geworden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

