
Wetenschap
Etheen versus ethaanoplosbaarheid in zwavelzuur:het verschil begrijpen
1. De rol van de dubbele binding in etheen
* Etheen's dubbele binding: Etheen bevat een dubbele koolstof-koolstofbinding. Deze dubbele binding is elektronenrijk, wat betekent dat deze een hoge concentratie elektronen heeft.
* Elektrofiele aanval: Geconcentreerd zwavelzuur is een sterk elektrofiel, wat betekent dat het wordt aangetrokken door elektronenrijke gebieden. De dubbele binding in etheen fungeert als een plaats voor elektrofiele aanval door het zwavelzuur.
2. De reactie met zwavelzuur
* Vorming van een tussenproduct: Het elektrofiele zwavelzuur valt de dubbele binding in etheen aan, verbreekt de dubbele binding en vormt een carbokation (een positief geladen koolstofatoom). Deze carbokation wordt vervolgens aangevallen door het sulfaation (SO4 2- ) om een alkylwaterstofsulfaatester te vormen.
* Oplosbaarheid: Deze alkylwaterstofsulfaatester is oplosbaar in geconcentreerd zwavelzuur vanwege zijn polaire aard en de vorming van waterstofbruggen.
3. Waarom ethaan niet oplost
* Geen dubbele binding: Ethaan heeft slechts enkele bindingen, wat betekent dat het de elektronenrijke dubbele binding mist die essentieel is voor de elektrofiele aanval door zwavelzuur.
* Niet-polair: Ethaan is een niet-polair molecuul. Geconcentreerd zwavelzuur is een polair oplosmiddel, en "het soort lost het soort op." Het gebrek aan polariteit in ethaan verhindert dat het oplost in het polaire zwavelzuur.
Samengevat:
Het belangrijkste verschil ligt in de reactiviteit van de twee moleculen. De dubbele binding van etheen maakt een reactie met geconcentreerd zwavelzuur mogelijk, waardoor een oplosbaar product ontstaat. Ethaan, dat geen dubbele binding heeft, reageert niet en blijft daarom onoplosbaar.
 Welke chemische stof op het periodiek systeem houdt niet van munten of bankbiljetten?
Welke chemische stof op het periodiek systeem houdt niet van munten of bankbiljetten?  Zijn de zuren uit wortels die gesteente afbreken een voorbeeld van mechanische verwering?
Zijn de zuren uit wortels die gesteente afbreken een voorbeeld van mechanische verwering?  Uit onderzoek blijkt hoe Rembrandt baanbrekend werk verrichtte met het impregneren van canvas op loodbasis voor De Nachtwacht
Uit onderzoek blijkt hoe Rembrandt baanbrekend werk verrichtte met het impregneren van canvas op loodbasis voor De Nachtwacht  Een scheutje zout kan MXene-supermaterialen versterken tegen oxidatie
Een scheutje zout kan MXene-supermaterialen versterken tegen oxidatie Enzymconformatie beïnvloedt de prestaties van lipase-aangedreven nanomotoren
Enzymconformatie beïnvloedt de prestaties van lipase-aangedreven nanomotoren
 Liefdadigheidsgiften:welke invloed hebben macht en overtuigingen over gelijkheid op donaties?
Liefdadigheidsgiften:welke invloed hebben macht en overtuigingen over gelijkheid op donaties?  Menselijke impact op het ecosysteem van Nieuw-Zeeland
Menselijke impact op het ecosysteem van Nieuw-Zeeland  Maïs met een laag gras:de beste combinatie vinden voor maïs op biobrandstof, bodembescherming
Maïs met een laag gras:de beste combinatie vinden voor maïs op biobrandstof, bodembescherming Maakt luchtvervuiling je ziek? 4 vragen beantwoord
Maakt luchtvervuiling je ziek? 4 vragen beantwoord Studie van Redoubt en andere vulkanen verbetert de detectie van onrust
Studie van Redoubt en andere vulkanen verbetert de detectie van onrust
Hoofdlijnen
- Hoe symboliseer je een dominant gen?
- Wat kunt u afleiden uit het feit dat het verdwijnen van slechts één soort een hele voedselketen verstoort?
- Welke korrelachtige structuren maken en bewaren eiwitten?
- Welke groep organismen wordt gevonden in oceanen en gebruiken stekende cellen genaamd cnidocyten om prooi te vangen?
- Hoe kan onderzoekers correcte informatie verkrijgen?
- Wat wordt veroorzaakt door genenstroom?
- Wat is het proces in welke cellen zich verdelen van twee nieuwe cellen?
- Twee eiwitten behouden de pluripotentie van embryonale stamcellen op verschillende manieren
- Wat gebeurt er als weefsel wordt aangevallen door een virus?
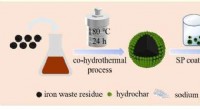
- Wetenschappers gebruiken tabaksafvalvloeistof en ijzerafval voor het verwijderen van Cd(II)
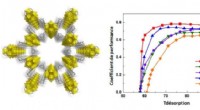
- Methoden voor machinaal leren bieden nieuwe inzichten in organisch-anorganische interfaces

- Chemici doen historische ontdekking van fluor

- Hoe het aantal neutronen te bepalen met behulp van het periodiek systeem

- Zeer efficiënte koeling met behulp van een nieuwe nanoporeuze vaste stof
 Verstoort klimaatverandering maritieme grenzen?
Verstoort klimaatverandering maritieme grenzen? Wat zou er gebeuren als elektriciteit duurder werd?
Wat zou er gebeuren als elektriciteit duurder werd?  Waterkrachtdammen kunnen kustgebieden ver benedenstrooms schaden
Waterkrachtdammen kunnen kustgebieden ver benedenstrooms schaden Waar komt in het menselijk lichaam osmose op?
Waar komt in het menselijk lichaam osmose op?  Werkstress bedreigt lerarenaanbod:RAND-enquête
Werkstress bedreigt lerarenaanbod:RAND-enquête ILL D20s neutronenbundel levert belangrijke aanwijzingen voor de onconventionele oorsprong van supergeleiding
ILL D20s neutronenbundel levert belangrijke aanwijzingen voor de onconventionele oorsprong van supergeleiding Wat is de Angular Resolution -formule in de astronomie en hoe beïnvloedt deze de duidelijkheid van hemelse observaties?
Wat is de Angular Resolution -formule in de astronomie en hoe beïnvloedt deze de duidelijkheid van hemelse observaties?  Een nieuwe manier om kosmische zwarte gaten te meten
Een nieuwe manier om kosmische zwarte gaten te meten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

