
Wetenschap
Volledige reactie verifiëren:ammoniak- en salpeterzuurresidu verwijderen
De reactie begrijpen:
* Ammoniak (NH3) en salpeterzuur (HNO3) reageren en vormen ammoniumnitraat (NH4NO3):
NH3 (water) + HNO3 (water) → NH4NO3 (water)
Methoden om ervoor te zorgen dat er geen reactanten achterblijven:
1. Stoichiometrie en overtollige reactanten:
* Bereken de exacte stoichiometrische verhouding: Dit is de ideale verhouding van ammoniak en salpeterzuur die nodig is voor een volledige reactie.
* Gebruik een overmaat van één reactant: Door opzettelijk meer van de ene reactant toe te voegen dan nodig is, zorg je ervoor dat de andere reactant volledig wordt verbruikt. Dit is een algemene strategie.
* Voorbeeld: Als je 1 mol ammoniumnitraat wilt maken, heb je 1 mol ammoniak en 1 mol salpeterzuur nodig. Je kunt 1,1 mol ammoniak toevoegen om ervoor te zorgen dat al het salpeterzuur reageert.
2. Titratie:
* Gebruik een pH-indicator: Ammoniak is basisch en salpeterzuur is zuur. Door de pH van het reactiemengsel te controleren, kunt u bepalen wanneer de oplossing een neutrale pH heeft bereikt, wat aangeeft dat beide reactanten zijn verbruikt.
3. Chemische tests:
* Test op ammoniak: Ammoniumzouten kunnen worden gedetecteerd door het reactiemengsel te verwarmen. Als er ammoniakgas vrijkomt, duidt dit op de aanwezigheid van niet-gereageerde ammoniak.
* Test op salpeterzuur: Salpeterzuur kan worden getest op lakmoespapier. Als het lakmoespapier rood wordt, duidt dit op de aanwezigheid van niet-gereageerd salpeterzuur.
4. Verdamping en kristallisatie:
* Verdamp het water: Ammoniumnitraat is een vaste stof. Door het water uit het reactiemengsel te verdampen, wordt eventueel achtergebleven ammoniak of salpeterzuur ook verdampt, waardoor alleen ammoniumnitraat overblijft.
* Kristalisatie: Ammoniumnitraat kristalliseert gemakkelijk. Als u de oplossing laat afkoelen en kristalliseren, wordt eventueel achtergebleven ammoniak of salpeterzuur uit de oplossing verwijderd.
Waarom dit belangrijk is:
* Zuiverheid van het product: Achtergebleven reagentia kunnen het product verontreinigen, waardoor het ongeschikt wordt voor het beoogde gebruik.
* Veiligheid: Sommige reactanten, zoals salpeterzuur, kunnen bijtend of gevaarlijk zijn. Door ervoor te zorgen dat ze volledig reageren, worden potentiële gevaren voorkomen.
* Opbrengst: Onvolledige reacties resulteren in lagere opbrengsten, wat betekent dat u minder van het gewenste product krijgt.
Belangrijke opmerkingen:
* Zorgvuldige controle: De bovenstaande methoden vereisen zorgvuldige monitoring en vereisen mogelijk aanpassingen op basis van de specifieke reactieomstandigheden.
* Veiligheidsmaatregelen: Hanteer chemicaliën altijd met passende veiligheidsmaatregelen, zoals het dragen van handschoenen en oogbescherming.
Laat het me weten als u een specifiek scenario in gedachten heeft, dan kan ik u meer advies op maat geven.
 Wat zijn fysieke kenmerken van etherische olie?
Wat zijn fysieke kenmerken van etherische olie?  Wat is het proces van een vaste wijze die rechtstreeks verandert in gas?
Wat is het proces van een vaste wijze die rechtstreeks verandert in gas?  Wat in een chemische formule vertelt hoeveel atomen van elk element eenheidsmaatschappijen worden gevonden?
Wat in een chemische formule vertelt hoeveel atomen van elk element eenheidsmaatschappijen worden gevonden?  Wat is het effect van chemische verandering en fysiek in de omgeving?
Wat is het effect van chemische verandering en fysiek in de omgeving?  Moet het EU-verbod op de import van zeehondenproducten standhouden?
Moet het EU-verbod op de import van zeehondenproducten standhouden?
Hoofdlijnen
- Heeft een bacteriecel membraan?
- Hoe helpen eiwitten ons?
- Welk deel van de cel is site -eiwitsynthese?
- Waarom neemt uw lichaam zuurstof in en transporteert u het naar cellen?
- Welke organel functioneert om eiwitten te verpakken en te leveren?
- Welke vorm van een eiwitmolecuul lijkt op?
- Kan water een cel binnendringen door actief transport?
- Zijn dieren kwetsbaar voor COVID-19?
- Hier ziet u hoe insecten planten ertoe aanzetten gallen te maken
- Wat onthult ijzeratoomnummer 26 over de structuur ervan?

- Zullen lithium-luchtbatterijen ooit vliegen?

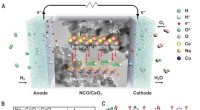
- Verlaging van de bedrijfstemperatuur van keramische brandstofcellen met een elektrolyt met hoge protongeleiding
- Nieuw polymeer met vormgeheugen betekent biomedische doorbraak

- Octapeptin:Vergeten antibioticum biedt hoop tegen de ergste superbacteriën
 Wat is een trillende boom?
Wat is een trillende boom?  Formaties die zijn ingeklemd tussen lagen bestaande rotsformaties die worden genoemd?
Formaties die zijn ingeklemd tussen lagen bestaande rotsformaties die worden genoemd?  Tot de kern van de zaak komen:Nanogels voor patiënten met een hartaanval
Tot de kern van de zaak komen:Nanogels voor patiënten met een hartaanval Cooler computergebruik door statistische fysica?
Cooler computergebruik door statistische fysica?  Waarom is kaliummanganaat 7 meer oplosbaar in hexaan dan water?
Waarom is kaliummanganaat 7 meer oplosbaar in hexaan dan water?  Chemici programmeren vloeibaar-kristallijne elastomeren om complexe draaibewegingen eenvoudig na te bootsen met behulp van licht
Chemici programmeren vloeibaar-kristallijne elastomeren om complexe draaibewegingen eenvoudig na te bootsen met behulp van licht Waarom heeft jouw boom dit najaar nog geen bladeren laten vallen, terwijl andere soortgelijke bomen dat wel hebben gedaan?
Waarom heeft jouw boom dit najaar nog geen bladeren laten vallen, terwijl andere soortgelijke bomen dat wel hebben gedaan?  Hoeveel gram ijs wordt er gevormd als 100 stoom in water en vervolgens in ijs verandert?
Hoeveel gram ijs wordt er gevormd als 100 stoom in water en vervolgens in ijs verandert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

