
Wetenschap
Hoeveel gram ijs wordt er gevormd als 100 stoom in water en vervolgens in ijs verandert?
1. Stoom naar water:
- Begintemperatuur van stoom:ongeveer 100°C (kookpunt van water)
- Eindtemperatuur van water:100°C (kookpunt van water)
- Latente verdampingswarmte (stoom naar water):L_v =2260 kJ/kg
De warmte die vrijkomt wanneer stoom condenseert tot water van 100°C wordt gegeven door:
Q_1 =m * L_v
waarbij m de massa van stoom is en Q_1 de vrijkomende warmte.
2. Water naar ijs:
- Begintemperatuur van water:100°C (kookpunt van water)
- Eindtemperatuur van ijs:0°C (vriespunt van water)
- Soortelijke warmtecapaciteit van water:c_w =4,18 kJ/kg °C
- Latente smeltwarmte (water naar ijs):L_f =334 kJ/kg
De warmte die vrijkomt wanneer water afkoelt van 100°C naar 0°C en vervolgens bevriest tot ijs, wordt gegeven door:
Q_2 =m * c_w * (100 - 0) + m * L_f
Omdat de warmte die vrijkomt tijdens de faseveranderingen (stoom in water en water in ijs) wordt gebruikt om 100 gram stoom in ijs om te zetten, kunnen we Q_1 en Q_2 gelijkstellen:
Q_1 =Q_2
m * L_v =m * c_w * (100 - 0) + m * L_f
Oplossen voor de massa van stoom (m):
m =(100 * c_w * 100 + 100 * L_f) / (L_v)
m =(41.800 kJ + 33.400 kJ) / (2260 kJ/kg)
m≈ 33,85 kg
Daarom zal 100 gram stoom ongeveer 33,85 kilogram ijs produceren wanneer het in water en vervolgens in ijs verandert.
 Zeldzaam ijzermineraal uit rotsen gevonden in weekdiertanden
Zeldzaam ijzermineraal uit rotsen gevonden in weekdiertanden Domino-achtige kristallisatie van glas
Domino-achtige kristallisatie van glas Onderzoekers tonen de impact van COVID-19 en klimaatverandering op de drinkwaterkwaliteit in Berlijn
Onderzoekers tonen de impact van COVID-19 en klimaatverandering op de drinkwaterkwaliteit in Berlijn  Ontdekking van een oermetabolisch systeem dat ons een glimp geeft van de oorsprong van het leven op aarde
Ontdekking van een oermetabolisch systeem dat ons een glimp geeft van de oorsprong van het leven op aarde Binnenkort:een bloedtest voor de ziekte van Alzheimer?
Binnenkort:een bloedtest voor de ziekte van Alzheimer?
Hoofdlijnen
- Onderzoek toont aan hoe embryonale stamcellen de menselijke ontwikkeling orkestreren
- Ziek van de Mexicaanse griep? Giftige algen kunnen de volgende grote bedreiging zijn
- Hoe de embryonale cellen van een worm zijn ontwikkelingspotentieel veranderen
- Gene drives hebben het potentieel om muggenpopulaties te onderdrukken, maar resistente muggen duiken op
- Wat is polyploïdie?
- Heerlijke narcissen zijn super eenvoudig te kweken. Hier is hoe
- Houden mannelijke vissen ze liever groot en kleurrijk?
- De oorsprong van het leven ontrafelen:vijf belangrijke doorbraken van de afgelopen vijf jaar
- De verbazingwekkende efficiëntie van het leven
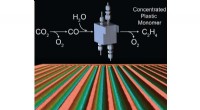
- Efficiënte elektrochemische cellen voor CO2-conversie
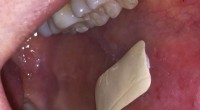
- Gips dat in de mond blijft plakken, kan de behandeling van orale aandoeningen verbeteren
- Slim materiaal maakt nieuwe toepassingen mogelijk in autonoom rijden en robotica

- Onderzoekers diversifiëren opties voor medicijnontwikkeling met nieuwe metaalkatalysator

- Een nieuwe brandstofcel-elektrolyt

 Feiten over vervuiling door plastic zak
Feiten over vervuiling door plastic zak  Vraag en antwoord:socioloog bespreekt waarom de carrières van vrouwen tijdens de pandemie meer hebben geleden dan die van mannen
Vraag en antwoord:socioloog bespreekt waarom de carrières van vrouwen tijdens de pandemie meer hebben geleden dan die van mannen Historische overstromingen laten zien hoe kwelders in de toekomst levens kunnen redden
Historische overstromingen laten zien hoe kwelders in de toekomst levens kunnen redden  Paleontologen beschrijven een conserveringsproces dat uniek is voor harsen
Paleontologen beschrijven een conserveringsproces dat uniek is voor harsen Metro-rijders in New York kunnen vanaf 31 mei het tarief aftappen en betalen
Metro-rijders in New York kunnen vanaf 31 mei het tarief aftappen en betalen Is cesiumcyanide oplosbaar in water?
Is cesiumcyanide oplosbaar in water?  Hoe kleurtemperatuur berekenen
Hoe kleurtemperatuur berekenen El Nino is terug, maar het is laat, zwak en waarschijnlijk geen probleem
El Nino is terug, maar het is laat, zwak en waarschijnlijk geen probleem
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

