
Wetenschap
Vlamtestkleuren:atomaire emissie begrijpen
1. Hitte en opwinding: Wanneer een metaalzout in een vlam wordt verwarmd, levert de hoge temperatuur voldoende energie om de elektronen in de metaalionen te exciteren. Deze elektronen springen naar hogere energieniveaus.
2. Terugkeren naar de grondstatus: Aangeslagen elektronen zijn onstabiel en willen terugkeren naar hun oorspronkelijke, lagere energieniveau (grondtoestand). Om dit te doen, geven ze de overtollige energie vrij als licht.
3. Unieke golflengten: Het energieverschil tussen de aangeslagen toestand en de grondtoestand is specifiek voor elk element. Dit energieverschil komt overeen met een specifieke golflengte van licht. Omdat verschillende elementen unieke energieniveaus hebben, zenden ze licht uit in verschillende kleuren.
Samengevat:
* Warmte: Levert energie voor elektronen om naar hogere niveaus te springen.
* Elektronenovergangen: Elektronen springen terug naar beneden en geven energie vrij als licht.
* Golflengte: De vrijkomende energie komt overeen met een specifieke golflengte van licht en bepaalt de kleur die we zien.
Voorbeeld:
* Natrium: Natriumionen zenden geel licht uit omdat het energieverschil tussen hun aangeslagen toestand en hun grondtoestand overeenkomt met de golflengte van geel licht.
* Koper: Koperionen zenden blauwgroen licht uit omdat het energieverschil voor koper zich in het blauwgroene deel van het zichtbare spectrum bevindt.
Belangrijke opmerking: De kleur die bij een vlamtest wordt waargenomen, kan worden beïnvloed door factoren zoals de aanwezigheid van andere elementen in het monster en de temperatuur van de vlam. Het principe van elektronische overgangen blijft echter hetzelfde, waardoor voor elk element een unieke "vingerafdruk" ontstaat.
Hoofdlijnen
- Hoe komt het nuttig vaker voor in een organisme in de loop van de tijd?
- Een eenvoudig diercelmodel maken
- Welke andere organismen maken lucht?
- Stimuleer stereotypen consumentenaankopen bij organisaties met of zonder winstoogmerk?
- Wat is het belang van microbiologie in de computer?
- Wat is de bijnaam voor mitochondria?
- Wat zijn de drie soorten afval die lichaam produceert?
- Wat is het meest voorkomende molecuul dat in een menselijk lichaam wordt gevonden?
- Een 'aardbeving' in de cel:wetenschappers ontdekken hoe een wijziging van de nucleaire lamina zijn vorm behoudt
- Het toepassen van computationele chemie om realistische chemische processen te simuleren

- Energie besparen bij de productie van chemicaliën

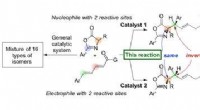
- Bepaal de creatie van chiraliteit door organische katalysatoren
- Sleutelcriteria voor het opstellen van een robuuste wetenschappelijke hypothese
- Moleculaire interacties meten
 Kernreactorbrandstoffen:uranium en plutonium begrijpen
Kernreactorbrandstoffen:uranium en plutonium begrijpen  Waar werd kinetische energie ontdekt?
Waar werd kinetische energie ontdekt?  Welke sterrenbeelden staan naast Leo de leeuw?
Welke sterrenbeelden staan naast Leo de leeuw?  De continenten drijven in de bovenste mantel vanwege een vorm van drijfvermogen bekend als?
De continenten drijven in de bovenste mantel vanwege een vorm van drijfvermogen bekend als?  Nieuwe ATLAS-precisiemetingen van het Higgs-boson in het gouden kanaal
Nieuwe ATLAS-precisiemetingen van het Higgs-boson in het gouden kanaal Waarom koude ijs in een andere stof overdragen?
Waarom koude ijs in een andere stof overdragen?  Leidinggevenden die gericht zijn op andere behoeften krijgen voordeel van de twijfel van werknemers, studie toont
Leidinggevenden die gericht zijn op andere behoeften krijgen voordeel van de twijfel van werknemers, studie toont Van broeikasgassen tot plastic:nieuwe katalysator voor recycling koolstofdioxide ontdekt
Van broeikasgassen tot plastic:nieuwe katalysator voor recycling koolstofdioxide ontdekt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


