
Wetenschap
Thermochemische tekenconventie:de warmtestroom begrijpen
* Warmte geabsorbeerd door het systeem: Positief (+)
* Warmte die vrijkomt door het systeem: Negatief (-)
Hier is een overzicht:
Systeem: Het systeem verwijst naar het specifieke deel van het universum dat je bestudeert, zoals een chemische reactie.
Omgeving: De omgeving is al het andere buiten het systeem.
Warmtestroom: Warmte kan tussen het systeem en de omgeving stromen.
Endotherme reactie: Een reactie die absorbeert warmte uit de omgeving. Het systeem wint energie en de enthalpieverandering (ΔH) is positief .
Exotherme reactie: Een reactie die loslaat warmte naar de omgeving. Het systeem verliest energie en de enthalpieverandering (ΔH) is negatief .
Voorbeelden:
* Smeltend ijs: Het ijs absorbeert warmte uit de omgeving en wordt vloeibaar water. Dit is een endotherm proces, ΔH> 0.
* Brandstof verbranden: De brandende brandstof geeft warmte af aan de omgeving. Dit is een exotherm proces, ΔH <0.
Belangrijke opmerking: Deze conventie wordt algemeen aanvaard in de scheikunde, maar het is van cruciaal belang om de specifieke context van elke thermochemische berekening te controleren om de gebruikte conventie te bevestigen.
 Wat is de eqatie voor calciumchloride en aluminiumsulfaat Welk type rectie is dit?
Wat is de eqatie voor calciumchloride en aluminiumsulfaat Welk type rectie is dit?  Wat zijn de kokende en smeltpunten van alkalische aardmetaal?
Wat zijn de kokende en smeltpunten van alkalische aardmetaal?  Hoe kunnen benzine en kerosine van elkaar worden gescheiden wanneer ze samengaan, het verschil tussen hun kookpunten is 25 graden Celsius?
Hoe kunnen benzine en kerosine van elkaar worden gescheiden wanneer ze samengaan, het verschil tussen hun kookpunten is 25 graden Celsius?  Wat is de toestandsverandering van gas naar vloeistof?
Wat is de toestandsverandering van gas naar vloeistof?  Hoeveel buitenste orbitale elektronen worden gevonden in een atoom van stikstof?
Hoeveel buitenste orbitale elektronen worden gevonden in een atoom van stikstof?
 Vijvers voor stormwaterbeheer bieden mogelijk geen oplossing voor het uitputten van wetlands
Vijvers voor stormwaterbeheer bieden mogelijk geen oplossing voor het uitputten van wetlands Een groene revolutie:hoe bossen veranderen en wat het betekent voor de planeet
Een groene revolutie:hoe bossen veranderen en wat het betekent voor de planeet  Opinie:Brazilië moet zijn overgebleven ongecontacteerde inheemse Amazones beschermen
Opinie:Brazilië moet zijn overgebleven ongecontacteerde inheemse Amazones beschermen Het Great Barrier Reef heeft de helft van zijn koralen verloren
Het Great Barrier Reef heeft de helft van zijn koralen verloren VN-chef gaat terug naar Caribisch gebied om alarm te slaan over klimaatverandering, orkanen
VN-chef gaat terug naar Caribisch gebied om alarm te slaan over klimaatverandering, orkanen
Hoofdlijnen
- Wat bepaalt een kenmerk in Gene?
- Wat is het meest gespecialiseerde orgaan in het lichaam?
- Wat is de wetenschappelijke naam voor ovaal blad?
- Hoe kan een mutatie geen invloed hebben op een organismen?
- Cytoplasma:de vitale vloeistof voor cellulair metabolisme
- Welke levensfunctie is primair betrokken bij de omzetting van in energie opgeslagen organische moleculen naar een vorm die direct bruikbaar is voor de cel?
- Kan het beschermen van onze eiwitten ons helpen veroudering te voorkomen?
- Hoe komt osmose voor in cellen?
- Plantencellen zijn totipotent, welke betekent?
- High-speed FM-AFM en simulatie onthullen atomaire oplossingsprocessen van calciet in water

- Micro-/nano-architecturen in MOF-membraan versnellen olie-waterscheiding

- Een bondgenoot voor legeringen:AI helpt bij het ontwerpen van hoogwaardig staal

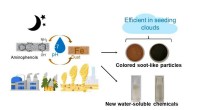
- Nieuwe chemie ontstaat wanneer stof vervuiling ontmoet
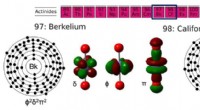
- Zeer zware elementen leveren meer elektronen
 Oleo Sponge succesvol in echte omstandigheden voor de kust van Californië
Oleo Sponge succesvol in echte omstandigheden voor de kust van Californië Hoe communicatie over milieukwesties de politieke kloof kan overbruggen
Hoe communicatie over milieukwesties de politieke kloof kan overbruggen  Is fruitcake een oplossingssuspensie of een mechanisch mengsel?
Is fruitcake een oplossingssuspensie of een mechanisch mengsel?  Kleuters kunnen meer rekenen dan je denkt
Kleuters kunnen meer rekenen dan je denkt Waarom moet de lift gelijk zijn aan de zwaartekracht in een vliegtuig?
Waarom moet de lift gelijk zijn aan de zwaartekracht in een vliegtuig?  Wat is het dichtstbijzijnde punt op aarde tot zon?
Wat is het dichtstbijzijnde punt op aarde tot zon?  Is Bromine een sterk of zwak zuur?
Is Bromine een sterk of zwak zuur?  Waarom zijn er maar weinig of geen wolken in de troposfeer?
Waarom zijn er maar weinig of geen wolken in de troposfeer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

