
Wetenschap
Koolstofallotropen:onderzoek naar diamant, grafiet en meer
1. Diamant: Een zeer harde en transparante vorm van koolstof waarbij elk koolstofatoom gebonden is aan vier andere koolstofatomen in een tetraëdrische structuur. Deze sterke binding maakt diamanten tot het hardste natuurlijk voorkomende materiaal.
2. Grafiet: Een zachte, zwarte en schilferige vorm van koolstof waarbij koolstofatomen zijn gerangschikt in lagen van zeshoekige ringen. Deze lagen zijn zwak gebonden, waardoor grafiet een goed smeermiddel en een geleider van elektriciteit is.
3. Fullereen: Een familie van koolstofmoleculen met gesloten kooistructuren, waarvan Buckminsterfullereen (C60) de bekendste is, die op een voetbal lijkt. Fullerenen hebben unieke eigenschappen en potentiële toepassingen op verschillende gebieden.
Andere allotrope vormen van koolstof zijn onder meer:
* Amorfe koolstof: Een niet-kristallijne vorm van koolstof met een ongeordende structuur, zoals roet en houtskool.
* Koolstofnanobuisjes: Cilindrische structuren van opgerolde grafeenplaten met uitzonderlijke sterkte en elektrische geleidbaarheid.
* Grafeen: Een enkele laag koolstofatomen gerangschikt in een zeshoekig rooster, bekend om zijn sterkte, geleidbaarheid en flexibiliteit.
Dus hoewel er gewoonlijk drie allotrope vormen worden genoemd, zijn er nog vele andere, elk met unieke eigenschappen en toepassingen.
 Wat is de procentuele samenstelling van calciumfluoride?
Wat is de procentuele samenstelling van calciumfluoride?  Wat is het verband tussen bijen- en wespensteken en zure alkaliën?
Wat is het verband tussen bijen- en wespensteken en zure alkaliën?  Wat is de belangrijkste regulator van CO2 in de atmosfeer omdat het gemakkelijk desolt?
Wat is de belangrijkste regulator van CO2 in de atmosfeer omdat het gemakkelijk desolt?  Ultrarekbare en vervormbare biosondes met Kirigami-ontwerpen
Ultrarekbare en vervormbare biosondes met Kirigami-ontwerpen Ontdekken hoe T-cellen het SARS-COV-2 virus spike-eiwit herkennen
Ontdekken hoe T-cellen het SARS-COV-2 virus spike-eiwit herkennen
Hoofdlijnen
- Welk organisme voert geen fotosynthese uit?
- Hoe worden enzymen beïnvloed door de omgeving?
- Wat is een Sugardoodle?
- Wat betekent TDF in de biologie?
- Een organisme zoals bacterie dat bestaat uit een enkele cel zonder kern is een?
- Wat is het eindproduct van fotosynthese? Een duidelijk overzicht
- Wat zijn de matrijzen die je van bacteriën kunt krijgen?
- Waarom lijden 600 meisjes in Mexico aan collectieve hysterie?
- Waarom restaurants willen dat je eten bestelt op je telefoon
- Bestrijding van kunstmatige trilhaartjes met magnetische velden en licht

- Materiaal met hoge brekingsindex behoudt een hoge doorlaatbaarheid na uitgloeien bij 850 ° C

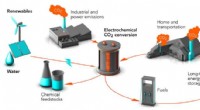
- Kunststoffen, brandstoffen en chemische grondstoffen uit CO2? Ze werken eraan
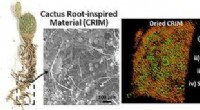
- Cactuswortels inspireren tot creatie van waterhoudend materiaal
- E. coli gebruiken om bioproducten te maken, zoals biodiesel, op een kosteneffectieve manier

 Ant-adaptatie
Ant-adaptatie  Wat wordt er gevormd uit gametophytes?
Wat wordt er gevormd uit gametophytes?  Bedrijven die blijk geven van toewijding aan duurzaamheid, inspireren groenere klanten
Bedrijven die blijk geven van toewijding aan duurzaamheid, inspireren groenere klanten  Welke spiegel wordt gebruikt in de grote binoculaire telescoop?
Welke spiegel wordt gebruikt in de grote binoculaire telescoop?  Wat zijn enkele voorbeelden van sterren die al in zwarte gaten zijn veranderd?
Wat zijn enkele voorbeelden van sterren die al in zwarte gaten zijn veranderd?  Diffusie en detectie op afstand van hete dragers in grafeen
Diffusie en detectie op afstand van hete dragers in grafeen Kunnen Dungeness-krab en zeegras het beheer van onze mariene hulpbronnen helpen verbeteren?
Kunnen Dungeness-krab en zeegras het beheer van onze mariene hulpbronnen helpen verbeteren?  Associatieve eigenschappen beheersen:een kindvriendelijke gids voor optellen, vermenigvuldigen en meer
Associatieve eigenschappen beheersen:een kindvriendelijke gids voor optellen, vermenigvuldigen en meer
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

