
Wetenschap
Periodieke tabelgroepen:vergelijkbare chemische eigenschappen begrijpen
Dit is waarom:
* Valentie-elektronen: Dit zijn de elektronen in de buitenste schil van een atoom. Zij zijn degenen die betrokken zijn bij chemische binding.
* Chemische binding: De manier waarop elementen met elkaar interageren, wordt voornamelijk bepaald door hoe hun valentie-elektronen zich gedragen.
* Vergelijkbare valentie-elektronenconfiguratie: Elementen in dezelfde groep delen hetzelfde aantal valentie-elektronen en hebben vaak vergelijkbare rangschikkingen van deze elektronen. Dit resulteert in vergelijkbare reactiviteitspatronen.
Voorbeeld:
* Groep 1 (Alkalimetalen):Alle alkalimetalen hebben één valentie-elektron. Dit maakt ze zeer reactief, omdat ze de neiging hebben dit elektron te verliezen en een +1 kation te vormen.
* Groep 17 (Halogenen):Alle halogenen hebben zeven valentie-elektronen. Ze hebben de neiging om één elektron te winnen om een -1 anion te vormen.
Samengevat:
Het vergelijkbare aantal en de rangschikking van valentie-elektronen binnen een groep leidt tot soortgelijke:
* Reactiviteit: Hoe gemakkelijk vormen ze banden met andere elementen.
* Oxidatietoestanden: De lading die ze doorgaans hebben bij het vormen van ionen.
* Soorten verbindingen: De soorten chemische verbindingen die ze vormen.
Hoewel elementen binnen een groep veel overeenkomsten vertonen, kunnen hun eigenschappen ook enigszins variëren als gevolg van verschillen in atomaire grootte en elektronegativiteit naarmate je verder in de groep komt.
 Wat is de kleinste eenheid van een verbinding? Moleculen begrijpen
Wat is de kleinste eenheid van een verbinding? Moleculen begrijpen  Onderzoekers gebruiken drukgevoelige moleculaire materialen om koeltechnologie te benutten
Onderzoekers gebruiken drukgevoelige moleculaire materialen om koeltechnologie te benutten Wat is gladde koolstof?
Wat is gladde koolstof?  Zink, een essentieel sporenelement voor de meeste organismen, is aanwezig op de actieve plaats van het enzym carboxypeptidase. Het zink functioneert waarschijnlijk als?
Zink, een essentieel sporenelement voor de meeste organismen, is aanwezig op de actieve plaats van het enzym carboxypeptidase. Het zink functioneert waarschijnlijk als?  Op maat gemaakte synthese van cyclische chemicaliën door middel van enzymen
Op maat gemaakte synthese van cyclische chemicaliën door middel van enzymen
Hoofdlijnen
- Wat zijn de soorten dichte bindweefsels?
- Onderzoekers ontdekken hoe mierensoorten hun buik gebruiken voor extra kracht tijdens sprongen
- Welk weefseltype is het meest betrokken bij het reguleren en beheersen van lichaamsfuncties?
- Onderzoekers zoeken burgerwetenschappers om bij te dragen aan het wereldwijd opsporen van muggen
- Bezuinigingen op het behoud brengen de Amazone-dieren in Brazilië in gevaar
- Wat wordt gemaakt van lipiden en diffunderen vrij in cellen door het plasma?
- Welke klier produceert de eiercellen en hormonen?
- Wat stimuleert de omzetting van glycogeen in glucose?
- Wat zijn de 4 belangrijkste delen van een bloem?
- Onderzoek kan ongewenste bijwerkingen bij nieuwe medicijnen minimaliseren

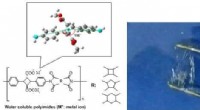
- Hoog-thermoresistente biopolyimiden worden in water oplosbaar zoals zetmeel
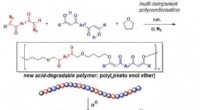
- Nieuw synthetisch polymeer afbreekbaar onder zeer milde zure omstandigheden
- Video:Hoe kom je van die stinkdiergeur af?

- De oorsprong van oppervlakteruwheid:atoomvervorming binnen en op het oppervlak van een vaste stof

 Wat betekent de terrestrische megafauna?
Wat betekent de terrestrische megafauna?  Welke deeltjes bevinden zich in de kern?
Welke deeltjes bevinden zich in de kern?  Verdwijnende koolstofcircuits op grafeen kunnen veiligheid bieden, biomedische toepassingen
Verdwijnende koolstofcircuits op grafeen kunnen veiligheid bieden, biomedische toepassingen Wat is de volgorde van planeten van Sun Out?
Wat is de volgorde van planeten van Sun Out?  Hoe zout bacteriën doodt:osmose uitgelegd en dagelijkse toepassingen
Hoe zout bacteriën doodt:osmose uitgelegd en dagelijkse toepassingen  Wat is de juiste volgorde van de nucleaire vervalmodus voor wijzigingen van U-238 naar U-234?
Wat is de juiste volgorde van de nucleaire vervalmodus voor wijzigingen van U-238 naar U-234?  Welke gevolgen heeft een droogte voor de aarde?
Welke gevolgen heeft een droogte voor de aarde?  'S Werelds eerste 5G-telefoon uitgebracht in Zuid-Korea
'S Werelds eerste 5G-telefoon uitgebracht in Zuid-Korea
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

