
Wetenschap
IJzer(III)oxide (Fe₂O₃):is het moleculair? Ionische binding begrijpen
* Ionische binding: IJzer(III)oxide (Fe₂O₃) wordt gevormd door ionische binding. IJzer (Fe) verliest drie elektronen om een positief geladen ion (Fe³⁺) te worden, terwijl zuurstof (O) er twee elektronen bij krijgt om een negatief geladen ion (O²⁻) te worden. Deze tegengesteld geladen ionen trekken elkaar elektrostatisch aan en vormen een kristalroosterstructuur.
* Geen discrete moleculen: In ionische verbindingen zijn er geen afzonderlijke, onafhankelijke moleculen. In plaats daarvan zijn de ionen in een zich herhalend patroon door het hele kristal gerangschikt. Er bestaat geen enkel ‘molecuul’ Fe₂O₃.
In tegenstelling daarmee:
* Moleculaire verbindingen: Moleculaire verbindingen worden gevormd door het delen van elektronen tussen atomen (covalente binding). Dit resulteert in duidelijke, afzonderlijke moleculen met een specifiek aantal atomen. Voorbeelden hiervan zijn water (H₂O) en kooldioxide (CO₂).
Daarom wordt ijzer(III)oxide beschouwd als een ionische verbinding en niet als een moleculaire verbinding.
 Opwarming van de Noordpool stimuleert strijd om rijkdom, scheepvaartroutes
Opwarming van de Noordpool stimuleert strijd om rijkdom, scheepvaartroutes Vergif of medicijnen? Cyanobacteriëngifstoffen beschermen kleine meerbewoners tegen parasieten
Vergif of medicijnen? Cyanobacteriëngifstoffen beschermen kleine meerbewoners tegen parasieten  Een nieuwe elektrochemische benadering zou de zuurgraad van de oceaan kunnen verminderen en daarbij koolstof kunnen verwijderen
Een nieuwe elektrochemische benadering zou de zuurgraad van de oceaan kunnen verminderen en daarbij koolstof kunnen verwijderen  Hoe een kust vol met schepen, havenstilstand en een anker hebben mogelijk olieramp in Orange County veroorzaakt
Hoe een kust vol met schepen, havenstilstand en een anker hebben mogelijk olieramp in Orange County veroorzaakt China's afvalverbod zet Amerikaanse recycling op z'n kop - is het tijd om verbranding te heroverwegen?
China's afvalverbod zet Amerikaanse recycling op z'n kop - is het tijd om verbranding te heroverwegen?
Hoofdlijnen
- Wat zijn de vele kleinere moleculen die DNA vormen?
- Cellen moeten genexpressie reguleren, zodat genen alleen tot expressie worden gebracht wanneer de eiwitten nodig zijn?
- Waarom moeten organismen voedsel hebben?
- Onderzoekers ontdekken nieuw lantibioticum geproduceerd door stafylokokken
- Overleven slechts enkele organismen op hun omgeving waar of onwaar?
- Populaties van insecten en bacteriën kunnen snel evolueren omdat ze meestal een korte hebben?
- Wat zijn de basiseigenschappen van kankercellen?
- Wat is het verschil tussen genomische en bio -informatica?
- Kan een klein deeltje de plaag van het vergroenen van citrusvruchten tegengaan?
- Het verlichten van kleine eiwitten in levende cellen met behulp van labelling-tags met één residu
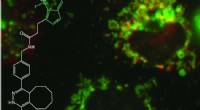
- Ingenieurs ontdekken nieuwe rol van water bij productie van hernieuwbare brandstoffen
- Onderzoek onthult de chemische onderbouwing van hoe goedaardig water kan veranderen in hard waterstofperoxide

- Onderzoekers onthullen hoe de MRSA-bacterie omgaat met stress

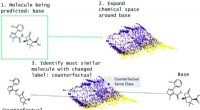
- Contrafeiten gebruiken om voorspellingen over de veiligheid van geneesmiddelen te verifiëren
 Als bacteriën die in zout zeewater wonen, worden verplaatst naar een zoetwateromgeving, is de celstructuur die zou voorkomen dat cellen scheuren?
Als bacteriën die in zout zeewater wonen, worden verplaatst naar een zoetwateromgeving, is de celstructuur die zou voorkomen dat cellen scheuren?  Hebben metalen een lage specifieke warmte?
Hebben metalen een lage specifieke warmte?  Geconfronteerd met de opwarming van de aarde, luchtvaart wil groen worden
Geconfronteerd met de opwarming van de aarde, luchtvaart wil groen worden Wat voor soort obligatie is FEO?
Wat voor soort obligatie is FEO?  Nieuwe microscooptechnologie geeft onderzoekers gedetailleerd inzicht in structuur en samenstelling van materialen
Nieuwe microscooptechnologie geeft onderzoekers gedetailleerd inzicht in structuur en samenstelling van materialen Nieuwe methode detecteert resterende verontreinigingen in ultrazuiver heliumgas
Nieuwe methode detecteert resterende verontreinigingen in ultrazuiver heliumgas Hoe beïnvloedt het niveau van zonnestraling dat op het oppervlak van verschillende delen arriveert het bioom dat zich daar bevindt?
Hoe beïnvloedt het niveau van zonnestraling dat op het oppervlak van verschillende delen arriveert het bioom dat zich daar bevindt?  Leven buiten de aarde - geen platentektoniek, geen probleem
Leven buiten de aarde - geen platentektoniek, geen probleem
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

