
Wetenschap
Ionische vergelijkingen in evenwicht brengen:Al + HCl - een stapsgewijze handleiding
1. Schrijf de onevenwichtige moleculaire vergelijking:
2 Al(s) + 6 HCl(aq) → 2 AlCl₃(aq) + 3 H₂(g)
2. Identificeer de toeschouwerionen:
Toeschouwerionen zijn ionen die aan beide kanten van de vergelijking voorkomen en niet deelnemen aan de daadwerkelijke reactie. In dit geval zijn de chloride-ionen (Cl⁻) toeschouwerionen.
3. Schrijf de volledige ionische vergelijking:
2 Al(s) + 6 H⁺(aq) + 6 Cl⁻(aq) → 2 Al³⁺(aq) + 6 Cl⁻(aq) + 3 H₂(g)
4. Annuleer de toeschouwerionen:
2 Al(s) + 6 H⁺(aq) → 2 Al³⁺(aq) + 3 H₂(g)
5. Vereenvoudig de vergelijking:
Al(s) + 3 H⁺(aq) → Al³⁺(aq) + 3/2 H₂(g)
Dit is de uitgebalanceerde ionische vergelijking voor de reactie van aluminium met zoutzuur.
Belangrijkste punten:
* Aluminium (Al) is een massief metaal.
*Zoutzuur (HCl) is een waterige oplossing.
* Aluminiumchloride (AlCl₃) is een waterige oplossing.
* Waterstofgas (H₂) wordt geproduceerd als gas.
* De coëfficiënten in de gebalanceerde vergelijking zorgen ervoor dat het aantal atomen van elk element aan beide kanten van de vergelijking hetzelfde is.
 Hoe werkt niet-permeabiliteit?
Hoe werkt niet-permeabiliteit?  Wat is het antwoord voor magnesium en carbonaat met behulp van de kriskras-methode?
Wat is het antwoord voor magnesium en carbonaat met behulp van de kriskras-methode?  Wat voor soort reacties zijn rode os -reacties?
Wat voor soort reacties zijn rode os -reacties?  Door elektriciteit aangedreven onderzeese reacties kunnen belangrijk zijn geweest voor het ontstaan van leven
Door elektriciteit aangedreven onderzeese reacties kunnen belangrijk zijn geweest voor het ontstaan van leven Ionen die zijn gemaakt van meer dan één atomen voorbeelden A.Neutral Iions B.positief c. negatief d. Polyatomische atomen?
Ionen die zijn gemaakt van meer dan één atomen voorbeelden A.Neutral Iions B.positief c. negatief d. Polyatomische atomen?
 NASA ziet post-tropische cycloon Helene Ierland treffen, Verenigd Koninkrijk
NASA ziet post-tropische cycloon Helene Ierland treffen, Verenigd Koninkrijk Houtskool:belangrijk ontbrekend stuk in de wereldwijde koolstofcyclus
Houtskool:belangrijk ontbrekend stuk in de wereldwijde koolstofcyclus Hoe meteorologen de volgende grote orkaan voorspellen
Hoe meteorologen de volgende grote orkaan voorspellen Het ondergrondse Parthenon dat Tokyo beschermt tegen overstromingen
Het ondergrondse Parthenon dat Tokyo beschermt tegen overstromingen Onderzoek naar manieren om de duurzaamheid te verbeteren en verspilling in de visindustrie te verminderen
Onderzoek naar manieren om de duurzaamheid te verbeteren en verspilling in de visindustrie te verminderen
Hoofdlijnen
- Een organisme bestaat uit twee lagencellen die een student die een met een samengestelde microscoop onder hoog vermogen observeert om de tweede laag te observeren?
- Chimpansees brengen insecten aan op wonden, een mogelijk geval van medicijngebruik?
- Wat zijn menselijke parasieten gevonden in urine?
- Hoe draagt geografische isolatie bij aan de evolutie van een nieuwe soort?
- Wat is proto-oncogeen?
- Wat is polycystronic mRNA?
- Somatische (volwassen) stamcellen:hun rollen, typen en therapeutisch potentieel
- Wat is een voorbeeld van de functie nerveus weefsel?
- Wat creëert eiwitten die door de cel worden gebruikt?
- Leuphana-wetenschappers ontwikkelen milieuvriendelijkere antibiotica

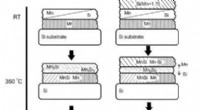
- Natuurkundigen houden toezicht op de vorming van hogere mangaansilicidefilms
- DNA uit sinaasappels halen:een eenvoudig, klaslokaalvriendelijk experiment

- Onderzoekers ontwikkelen flexibel kristal, de weg vrijmaken voor efficiëntere buigbare elektronica

- Hoe een waterbarometer te lezen:een praktische gids voor weersvoorspellingen

 De positieve kanten van klimaatverandering? Onderzoek toont aan dat landbouw, economische mogelijkheden
De positieve kanten van klimaatverandering? Onderzoek toont aan dat landbouw, economische mogelijkheden Hoe magneten te gebruiken om elektriciteit te geleiden
Hoe magneten te gebruiken om elektriciteit te geleiden  Wetenschappers stellen een nieuwe strategie voor om het celcommunicatienetwerk te reguleren
Wetenschappers stellen een nieuwe strategie voor om het celcommunicatienetwerk te reguleren Wat zou de meeste kinetische energie hebben, een hete gaskool vaste vloeistof of vloeistof?
Wat zou de meeste kinetische energie hebben, een hete gaskool vaste vloeistof of vloeistof?  Hoe heten de sterren waaruit Canis Major bestaat?
Hoe heten de sterren waaruit Canis Major bestaat?  Wanneer een element een ander atoomnummer en dezelfde massa heeft, hoe wordt het genoemd?
Wanneer een element een ander atoomnummer en dezelfde massa heeft, hoe wordt het genoemd?  Cassini-sonde vindt enorme leegte tussen de ringen van Saturnus
Cassini-sonde vindt enorme leegte tussen de ringen van Saturnus Fabricage van metamoleculen metamaterialen met 3D-co-assemblage
Fabricage van metamoleculen metamaterialen met 3D-co-assemblage
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

