
Wetenschap
Kooldioxide versus natriumoxide:een vergelijking van fysieke eigenschappen
Kooldioxide (CO2)
* Toestand bij kamertemperatuur: Gas
* Uiterlijk: Kleurloos en geurloos
* Dichtheid: 1,98 kg/m³ (bij 0 °C en 1 atm)
* Smeltpunt: -78,5 °C (-109,3 °F) (sublimeert)
* Kookpunt: -56,6 °C (-69,9 °F)
* Oplosbaarheid in water: Enigszins oplosbaar (vormt koolzuur)
* Geleidbaarheid: Niet-geleidend (in gasvorm)
Natriumoxide (Na2O)
* Toestand bij kamertemperatuur: Solide
* Uiterlijk: Witte, kristallijne vaste stof
* Dichtheid: 2,27 g/cm³
* Smeltpunt: 1275 °C (2327 °F)
* Kookpunt: 1950 °C (3542 °F)
* Oplosbaarheid in water: Reageert hevig met water en vormt natriumhydroxide (NaOH)
* Geleidbaarheid: Niet-geleidend in zijn vaste vorm, maar kan wel geleidend zijn als het in water wordt opgelost (vanwege de vorming van ionen)
Belangrijkste verschillen:
* Stand van zaken: CO2 is bij kamertemperatuur een gas, terwijl Na2O een vaste stof is.
* Smelt- en kookpunten: Na2O heeft veel hogere smelt- en kookpunten dan CO2 vanwege de sterke ionische bindingen die de structuur bij elkaar houden.
* Oplosbaarheid: CO2 is enigszins oplosbaar in water, terwijl Na2O heftig reageert met water, waardoor een sterk alkalische oplossing ontstaat.
* Geleidbaarheid: CO2 is een slechte geleider van elektriciteit, terwijl Na2O kan geleiden als het in water is opgelost.
Samengevat: De verschillen in fysische eigenschappen tussen koolstofdioxide en natriumoxide komen voort uit de verschillen in hun binding en moleculaire structuren. CO2 is een moleculaire verbinding met zwakke intermoleculaire krachten, terwijl Na2O een ionische verbinding is met sterke elektrostatische interacties tussen de ionen.
 Wat is de kleur van waterige broom na toevoeging koolwaterstof?
Wat is de kleur van waterige broom na toevoeging koolwaterstof?  Vriezen alle stoffen in vaste stoffen bij nul graden Celsius?
Vriezen alle stoffen in vaste stoffen bij nul graden Celsius?  Het soort attracties die resulteren in het oplossende natriumchloride water zijn?
Het soort attracties die resulteren in het oplossende natriumchloride water zijn?  Techniek onthult hoe kristallen zich vormen op oppervlakken
Techniek onthult hoe kristallen zich vormen op oppervlakken  Wat is het ijskoude en kookpunt voor water in Celsius?
Wat is het ijskoude en kookpunt voor water in Celsius?
Hoofdlijnen
- Is het ribosoom een plantaardige of dierlijke structuur?
- Wat zijn de overeenkomsten en verschillen tussen mitose -meiose met betrekking tot de functielocatie in het chromosoomnummer van het organisme haploïde of diploïde van geproduceerde dochtercellen?
- Uit onderzoek blijkt waarom de zebra zijn strepen kreeg
- Wat is een fylogenetisch classificatiesysteem dat gedeelde afgeleide karakters en afkomst gebruikt als het enige criterium voor het groeperen van taxa?
- Gedeelde kenmerken van eukaryotische en prokaryotische cellen
- UW-wetenschappers ontrafelen het mysterie van hoe griepvirussen zich vermenigvuldigen
- Wat zijn de vier basisonderdelen voor een menselijke cel?
- Wat is het somatische systeem?
- Wat zijn de componenten van het ecosysteem?
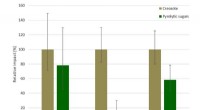
- Duurzaamheid van nieuw creosootalternatief bevestigd
- Uit onderzoek blijkt dat elk haar van het menselijk lichaam kan worden gebruikt voor identificatie

- Nieuwe manier om het elektrische dubbellaagse effect te onderzoeken
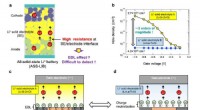
- Elektrochemische reductie van kooldioxide tot ethanol

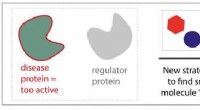
- Hoe moleculaire lijmen te vinden om ziekten effectief aan te pakken?
 Google koopt Fitbit in overstap naar wearables, digitale gezondheid
Google koopt Fitbit in overstap naar wearables, digitale gezondheid Wat is functiebasis in een microscoop?
Wat is functiebasis in een microscoop?  Toont een politieke of fysieke kaart u bergen rivieren en meren?
Toont een politieke of fysieke kaart u bergen rivieren en meren?  Welk type laag plat land dat achterblijft na een groot lichaamswater zoals meer is volledig verdwenen?
Welk type laag plat land dat achterblijft na een groot lichaamswater zoals meer is volledig verdwenen?  Waar vind je het grootste potentieel en kinetische energie op een slinger of achtbaan?
Waar vind je het grootste potentieel en kinetische energie op een slinger of achtbaan?  Wat is het verschil tussen een manier waarop een fossiele brandstoffenpunt elektriciteit en elektriciteit van kerncentrales genereert?
Wat is het verschil tussen een manier waarop een fossiele brandstoffenpunt elektriciteit en elektriciteit van kerncentrales genereert?  Verhoogde angst bij jonge zwarte volwassenen door blootstelling aan politiegeweld
Verhoogde angst bij jonge zwarte volwassenen door blootstelling aan politiegeweld Hoeveel meter zijn 27,5 killliometers?
Hoeveel meter zijn 27,5 killliometers?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

