
Wetenschap
Loodoxide:vorming, chemische reactie en typen
Hier is hoe het gebeurt:
1. Oxidatie: Lood (Pb) reageert gemakkelijk met zuurstof (O2) in aanwezigheid van warmte of lucht.
2. Chemische reactie: Bij de reactie verliest lood elektronen en zuurstof wint elektronen. Deze overdracht van elektronen vormt ionische bindingen, wat leidt tot de vorming van loodoxide.
Het specifieke type loodoxide dat wordt gevormd, hangt af van de reactieomstandigheden, waaronder de temperatuur en de aanwezige hoeveelheid zuurstof.
Hier zijn enkele veel voorkomende soorten loodoxiden:
* Lood(II)oxide (PbO): Ook bekend als litharge, het is een geel tot oranje poeder.
* Lood(IV)oxide (PbO2): Het is een donkerbruin poeder, dat vaak wordt gebruikt in loodzuuraccu's.
* Lood(II,IV)oxide (Pb3O4): Bekend als rood lood, het is een felrood poeder dat als pigment wordt gebruikt.
De reactie kan worden weergegeven door de volgende chemische vergelijkingen:
* Vorming van lood(II)oxide:
* 2Pb + O2 → 2PbO
* Vorming van lood(IV)oxide:
* Pb + O2 → PbO2
Loodoxide is een veelzijdige verbinding met verschillende toepassingen in verschillende industrieën, waaronder:
* Pigmenten: Gebruikt in verven, keramiek en glas.
* Batterijen: Gebruikt in loodzuurbatterijen.
* Elektronica: Gebruikt bij de productie van halfgeleiders.
* Rubber: Gebruikt als vulkaniseermiddel.
Het is belangrijk op te merken dat loodoxide een giftige stof is en dat er met zorg mee moet worden omgegaan.
 Mangaan(III)sulfaatformule:chemische formules begrijpen
Mangaan(III)sulfaatformule:chemische formules begrijpen  Hoe worden covalente bindingen bij elkaar gehouden?
Hoe worden covalente bindingen bij elkaar gehouden?  Wat zijn de 5 kenmerken van chemische verandering?
Wat zijn de 5 kenmerken van chemische verandering?  Uit onderzoek blijkt waarom de luchtvervuiling in het oosten van de VS in de winter meer stagneert
Uit onderzoek blijkt waarom de luchtvervuiling in het oosten van de VS in de winter meer stagneert  Draagt elektronen een negatieve en positieve lading?
Draagt elektronen een negatieve en positieve lading?
 Waarom bestaan er cruciale culturele verschillen tussen landen?
Waarom bestaan er cruciale culturele verschillen tussen landen?  Zinkende zeebergen maken en dempen aardbevingen
Zinkende zeebergen maken en dempen aardbevingen Tweederde van 's werelds langste rivieren gesmoord door de mensheid:studie
Tweederde van 's werelds langste rivieren gesmoord door de mensheid:studie Wanneer mensen behoud oefenen, hoe beïnvloeden ze het milieu?
Wanneer mensen behoud oefenen, hoe beïnvloeden ze het milieu?  Zijn diepblauwe zeeën aan het vervagen? Oceanen krijgen in delen van de aarde een nieuwe kleur, zo blijkt uit onderzoek
Zijn diepblauwe zeeën aan het vervagen? Oceanen krijgen in delen van de aarde een nieuwe kleur, zo blijkt uit onderzoek
Hoofdlijnen
- Welke biomen leven rode vossen?
- Insectenfrass wordt voedsel voor eiwitrijke microalgen
- Linnaeus gebruikte overeenkomsten in structuur om relaties tussen organismen of onwaar te bepalen?
- Welke plantcel heeft een muur?
- Er is een Y -vormige replicatievork aan elke kant van bubbel. Hoe worden de zijkanten genoemd?
- Wat is een reden waarom de classificatie van protisten in één koninkrijk moeilijk is?
- Wat zijn implicatie van T -celrespons?
- Wat is de definitie van evolutie?
- Terugkijken op de geschiktheid van het verhaal over het economisch beleid dat ten grondslag ligt aan de Groene Revolutie
- Selectief kooldioxide omzetten in methaan of ethaan

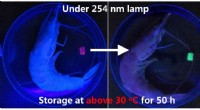
- Kunstmatig van kleur veranderend materiaal dat de huid van een kameleon nabootst, kan de versheid van zeevruchten detecteren
- Metaal-organische raamwerken kunnen ondanks de aanwezigheid van water gassen scheiden

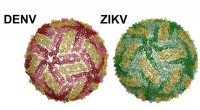
- Onderzoekers ontdekken hoe lichaamstemperatuur potentiële knokkelkoorts vernietigt, Zika-vaccin
- Onderzoekers kunnen rekenen op verbeterde proteomics-methode

 Welk orgaan kan ADH helpen bij het voorkomen van waterbehoud door interactie met doelcellen?
Welk orgaan kan ADH helpen bij het voorkomen van waterbehoud door interactie met doelcellen?  Een jet gaat van start. Het beweegt met 10,00 km per uur en versnelt naar 1000 H2 gedurende 30,0s Wat het laatste snelheid einde van 30,0s?
Een jet gaat van start. Het beweegt met 10,00 km per uur en versnelt naar 1000 H2 gedurende 30,0s Wat het laatste snelheid einde van 30,0s?  Is een complexe structurele organisatie niet kenmerkend voor levende organismen?
Is een complexe structurele organisatie niet kenmerkend voor levende organismen?  Waarom Instagram je mentale gezondheid kan beïnvloeden (en wat je eraan kunt doen)
Waarom Instagram je mentale gezondheid kan beïnvloeden (en wat je eraan kunt doen) Wanneer het zuur reageert met een carbonaat, wat zijn drie producten?
Wanneer het zuur reageert met een carbonaat, wat zijn drie producten?  Verstrengeling van fotonen van verschillende kleuren
Verstrengeling van fotonen van verschillende kleuren Hoe het luisteren naar Noord-Atlantische walvissen mensen kan helpen hen te beschermen
Hoe het luisteren naar Noord-Atlantische walvissen mensen kan helpen hen te beschermen  Welk materiaal gebruikt een kerncentrale voor energie?
Welk materiaal gebruikt een kerncentrale voor energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

