
Wetenschap
Neutraliserende zuren:reacties en pH-veranderingen begrijpen
Hier is een overzicht:
* Zuren: Ze hebben een pH lager dan 7, wat betekent dat ze een hoge concentratie waterstofionen (H+) hebben.
* Neutrale stoffen: Hebben een pH van 7, wat betekent dat ze een gelijke concentratie waterstof- en hydroxide-ionen (OH-) hebben.
* Basis: Een pH groter dan 7 hebben, wat betekent dat ze een hoge concentratie hydroxide-ionen (OH-) hebben.
Wat gebeurt er als je een neutrale stof aan een zuur toevoegt?
* Geen significante verandering in pH: De neutrale stof zal niet significant bijdragen aan de waterstof- of hydroxide-ionenconcentratie.
* Verdunning: Als je een stof aan een zuur toevoegt, wordt het zuur verdund, wat betekent dat de concentratie H+-ionen lichtjes afneemt. Deze pH-verandering is echter meestal gering, vooral als de toegevoegde hoeveelheid neutrale stof klein is.
* Potentieel voor reactie: In sommige gevallen kan de neutrale stof reageren met het zuur. Het toevoegen van water aan een sterk zuur zoals zwavelzuur kan bijvoorbeeld warmte genereren als gevolg van de reactie.
Voorbeelden van neutrale stoffen:
* Water (H2O)
* Suiker (C12H22O11)
* Zout (NaCl)
Belangrijke opmerking: Als je een base aan een zuur toevoegt, krijg je een neutralisatiereactie, waardoor de pH van de oplossing naar neutraliteit stijgt.
 Mensen dringen de laatste wilde plekken van Antarctica binnen, bedreigt de kwetsbare biodiversiteit
Mensen dringen de laatste wilde plekken van Antarctica binnen, bedreigt de kwetsbare biodiversiteit Waarom water en voedingsstoffen geabsorbeerd door reizen naar de stengels bladeren?
Waarom water en voedingsstoffen geabsorbeerd door reizen naar de stengels bladeren?  Wat beïnvloedt de natuurlijke selectie?
Wat beïnvloedt de natuurlijke selectie?  Effecten van aardgas beoordeeld in onderzoek naar schaliegasexplosie in Appalachian Basin
Effecten van aardgas beoordeeld in onderzoek naar schaliegasexplosie in Appalachian Basin Vergeet enorme zeeweringen - wetlands aan de kust bieden de beste bescherming tegen storm die u kunt kopen
Vergeet enorme zeeweringen - wetlands aan de kust bieden de beste bescherming tegen storm die u kunt kopen
Hoofdlijnen
- Gymnosperm-kegels:de zaaddragende structuur begrijpen
- Waarom worden mitochondria de Powers Houses of Cell genoemd?
- Welke twee dingen hebben wetenschappers geholpen meer details in cellen te zien?
- De ontwikkeling van nieuwe verbindingen tussen hersencellen wordt genoemd?
- Eenmaal uitgestorven verklaard, Lord Howe Island wandelende takken leven echt
- Wat is de gram vlek van gist?
- Hoe wordt het voedsel geleidend weefsel van een plant genoemd?
- Moleculaire modellen:hoe ze zich verhouden tot andere modellen
- Waarom is celvertaling nodig?
- Computationeel onderzoek beschrijft het activeringsmechanisme van p38-alpha

- Bouw een 3D-model van een natriumatoom:stapsgewijze handleiding

- Door bacteriële enzymen te kopiëren, lab leert snel nieuwe klasse antibiotica moleculen schoon te synthetiseren, efficiënt

- Zelfmontage, biomimetische composieten hebben ongebruikelijke elektrische eigenschappen
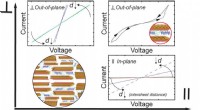
- Gigantische omkering van lading voor het eerst waargenomen

 Wat is het klimaat aan de oceaankant van een berg?
Wat is het klimaat aan de oceaankant van een berg?  Luchtverspreidingsmodellen voor geurbeoordeling
Luchtverspreidingsmodellen voor geurbeoordeling Verkeersopstoppingen heroverwogen
Verkeersopstoppingen heroverwogen Onderzoekers gebruiken van mosselen afkomstige eiwitten om op maat gemaakte bio-adhesieve onderwaterpleisters te ontwikkelen
Onderzoekers gebruiken van mosselen afkomstige eiwitten om op maat gemaakte bio-adhesieve onderwaterpleisters te ontwikkelen  Waar komt de geologie vandaan?
Waar komt de geologie vandaan?  Studie vindt geschiedenis van Titans landschap lijkt op dat van Mars, niet de aarde
Studie vindt geschiedenis van Titans landschap lijkt op dat van Mars, niet de aarde Concentratie van concentratie van gewichtspercentage naar massa per volume -eenheid?
Concentratie van concentratie van gewichtspercentage naar massa per volume -eenheid?  Zuurstof lossen in een RBC als gevolg van afnemende pH wordt het wat genoemd?
Zuurstof lossen in een RBC als gevolg van afnemende pH wordt het wat genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

