
Wetenschap
Bereken de hydroxide-ionenconcentratie op basis van de pH:een stapsgewijze handleiding
De relatie begrijpen
* pH en pOH: pH en pOH zijn aan elkaar gerelateerd via de volgende vergelijking:pH + pOH =14
* [H+] en [OH-] :De concentratie van waterstofionen ([H+]) en hydroxide-ionen ([OH-]) zijn ook gerelateerd aan de volgende vergelijking:[H+][OH-] =1,0 x 10^-14 (dit is de ionenproductconstante voor water, Kw)
Stappen om [OH-] te berekenen
1. Bereken pOH: Gebruik de vergelijking pH + pOH =14 om de pOH te vinden.
2. Bereken [OH-]: Gebruik de vergelijking pOH =-log[OH-] om de concentratie van hydroxide-ionen te vinden.
Voorbeeld:
Stel dat u een oplossing heeft met een pH van 10.
1. Bereken pOH:
pOH =14 - pH =14 - 10 =4
2. Bereken [OH-] :
[OH-] =10^-pOH =10^-4 M
Daarom is de concentratie hydroxide-ionen in een oplossing met een pH van 10 1,0 x 10^-4 M.
Belangrijke opmerkingen
* De eenheden voor concentratie zijn gewoonlijk molariteit (M), wat het aantal mol per liter (mol/L) vertegenwoordigt.
* Naarmate de pH stijgt, neemt de concentratie van hydroxide-ionen toe en wordt de oplossing basischer (alkalisch).
* Omgekeerd, als de pH daalt, neemt de concentratie van hydroxide-ionen af en wordt de oplossing zuurder.
 De groei van kolencentrales in Myanmar kan 280 doden, 000:studie
De groei van kolencentrales in Myanmar kan 280 doden, 000:studie Megadroughs hielpen oude rijken omver te werpen. Ze zijn in het verleden van Australië, en er komen er nog meer
Megadroughs hielpen oude rijken omver te werpen. Ze zijn in het verleden van Australië, en er komen er nog meer Deutsche Bank stopt met financiering kolenprojecten
Deutsche Bank stopt met financiering kolenprojecten De 2 belangrijkste componenten van een ecosysteem
De 2 belangrijkste componenten van een ecosysteem  Wat zijn de voordelen van huisvliegen?
Wat zijn de voordelen van huisvliegen?
Hoofdlijnen
- Wat zijn enkele dieren die consumenten op het 2e niveau in het oceaanecosysteem?
- Wat is het effect van verschillende soortenplanten die zeer DNA hebben?
- Bloedsomloop:hoe het de wortelfunctie van planten weerspiegelt
- Welke structuren zorgen voor celbeweging?
- H5N1-stam van vogelgriep gevonden in melk:WHO
- Tijdbesparende bodemtests voorspelt belangrijke kenmerken van de bodemgezondheid
- Hoe reproduceren Streptococcus -pyogenen zich?
- Wat heeft wetenschapper Linnaeus bijgedragen aan de plantkunde?
- Ongeveer 200 gestrande walvissen sterven in beukende branding in Australië
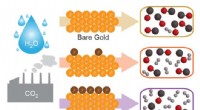
- Wetenschappers stemmen het systeem af om syngas te maken uit CO2
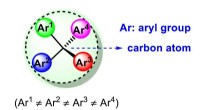
- Wetenschappers hebben nieuwe manier gevonden om chirale tetraarylmethaan te synthetiseren
- Materiaalinformatica onthult nieuwe klasse van superharde legeringen

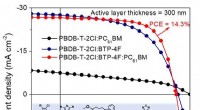
- Meer dan 14% efficiëntie voor ternaire organische zonnecel met 300 nm dikke actieve laag
- De 3 meter hoge microscopen helpen de ergste ziekten ter wereld te bestrijden

 Wolken zouden kunnen verklaren hoe Sneeuwbalaarde ontdooide
Wolken zouden kunnen verklaren hoe Sneeuwbalaarde ontdooide  Een bal wordt met voldoende snelheid recht omhoog gegooid, zodat deze enkele seconden in de lucht is wat zijn snelheid 2s voordat hij het hoogste punt bereikt?
Een bal wordt met voldoende snelheid recht omhoog gegooid, zodat deze enkele seconden in de lucht is wat zijn snelheid 2s voordat hij het hoogste punt bereikt?  NASA's Mars 2020 krijgt een dosis ruimte hier op aarde
NASA's Mars 2020 krijgt een dosis ruimte hier op aarde Biotechnologie werd de nieuwe grens in de geneeskunde door het ontrafelen van geheimen van het leven en deze code?
Biotechnologie werd de nieuwe grens in de geneeskunde door het ontrafelen van geheimen van het leven en deze code?  Kun je een boom vergelijken met het menselijk leven?
Kun je een boom vergelijken met het menselijk leven?  Wat zal hoogstwaarschijnlijk gebeuren met een plant die niet genoeg zonlicht doet herleven?
Wat zal hoogstwaarschijnlijk gebeuren met een plant die niet genoeg zonlicht doet herleven?  Is een legering een zuivere substantie van mengsel?
Is een legering een zuivere substantie van mengsel?  Wat is het proces dat resulteert in een toename van het atoomnummer?
Wat is het proces dat resulteert in een toename van het atoomnummer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

