
Wetenschap
Berekening van de pOH van ammoniak:een stapsgewijze handleiding
* Ammoniak is een zwakke base: Het ioniseert niet volledig in water, wat betekent dat het niet alle hydroxide-ionen (OH⁻) volledig afstaat.
* pOH hangt af van [OH⁻]: De pOH van een oplossing wordt berekend met behulp van de volgende formule:
pOH =-log[OH⁻]
Om de pOH van ammoniak te vinden, heb je nodig:
1. De concentratie ammoniak: Dit wordt meestal uitgedrukt in molariteit (M).
2. De Kb-waarde voor ammoniak: Dit is de basisionisatieconstante, die aangeeft in welke mate ammoniak in water ioniseert.
Zo bereken je de pOH:
1. Een ICE-tabel instellen: Dit zal u helpen de veranderingen in de concentratie te volgen terwijl ammoniak ioniseert.
```
NH₃(aq) + H₂O(l) ⇌ NH₄⁺(aq) + OH⁻(aq)
Initieel:[NH₃] 0 0
Wijzigen:-x +x +x
Equilib:[NH₃]-x x x
```
2. Schrijf de Kb-expressie:
Kb =([NH₄⁺][OH⁻]) / [NH₃]
3. Vervang de evenwichtsconcentraties uit de ICE-tabel en los x op:
Kb =(x * x) / ([NH₃] - x)
4. Oplossen voor [OH⁻]:
[OH⁻] =X
5. Bereken pOH:
pOH =-log[OH⁻]
Voorbeeld:
Stel dat u een 0,1 M-oplossing van ammoniak heeft, en de Kb voor ammoniak is 1,8 x 10⁻⁵. U volgt de bovenstaande stappen om de pOH te berekenen.
Onthoud: pOH is een maatstaf voor de concentratie hydroxide-ionen en is omgekeerd evenredig met de pH. Hoe hoger de pOH, hoe lager de hydroxideconcentratie en hoe zuurder de oplossing.
 Ogen in de lucht:hoe satellieten de gezondheid van de infrastructuur kunnen bewaken
Ogen in de lucht:hoe satellieten de gezondheid van de infrastructuur kunnen bewaken Op wie zijn producenten afhankelijk van een ecosysteem?
Op wie zijn producenten afhankelijk van een ecosysteem?  Houtverbruik bij energieopwekking blijft stijgen
Houtverbruik bij energieopwekking blijft stijgen Amazonewoud kan worden getraind door grotere variabiliteit in regenval
Amazonewoud kan worden getraind door grotere variabiliteit in regenval Fermi vangt gammaflitsen van tropische stormen
Fermi vangt gammaflitsen van tropische stormen
Hoofdlijnen
- Wat zijn de delen van een limaboon?
- Wetenschapper die voedingsstoffen ontdekte?
- De archeebacteriën waren waarschijnlijk de eerste wat?
- Wat is translocatie in de fysiologie?
- Wat bevindt zich in de kern en bevat DNA?
- Wat is één cel verdeeld in twee identieke dochtercellen?
- Welke structuur regelt de beweging van materialen in en uit alle cellen?
- De gamete die genen bevat die alleen door de moeder worden bijgedragen?
- Hoe komen de wetenschappers ten goede aan de samenleving?
- De deeltjesgrootte van nanodeeltjes van een Pt₅Ce-legering afstemmen op de zuurstofreductiereactie

- Wetenschappers ontdekken nieuwe niet-kleverige gels

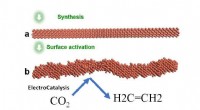
- Onderzoekers ontdekken effectieve manier om koolstofdioxide om te zetten in ethyleen
- De eindtemperatuur voorspellen in een calorimeter:een stapsgewijze handleiding

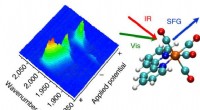
- Lasertechniek kan de deur openen naar efficiëntere schone brandstoffen
 Wanneer begint de Midden -Europese zomertijd?
Wanneer begint de Midden -Europese zomertijd?  Alternatieven voor Firebrick
Alternatieven voor Firebrick beïnvloeder, beroemdheid, journalist? Tieners wenden zich tot YouTube voor nieuws, enquête toont
beïnvloeder, beroemdheid, journalist? Tieners wenden zich tot YouTube voor nieuws, enquête toont Hoe een tRNA-reeks te krijgen van een DNA-reeks
Hoe een tRNA-reeks te krijgen van een DNA-reeks  Betekenis van de eerste H in het periodiek systeem?
Betekenis van de eerste H in het periodiek systeem?  We hebben zeven jaar lang de Britse politie geobserveerd en gefouilleerd. Dit is wat we hebben gevonden
We hebben zeven jaar lang de Britse politie geobserveerd en gefouilleerd. Dit is wat we hebben gevonden  Emirates kiest voor 30 Boeing 787 Dreamliners in herziene deal
Emirates kiest voor 30 Boeing 787 Dreamliners in herziene deal Gebruik de helium-4-isotoop om het atoomnummer en de massa te definiëren, waarom is een kennis van?
Gebruik de helium-4-isotoop om het atoomnummer en de massa te definiëren, waarom is een kennis van?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

