
Wetenschap
De pH van gedestilleerd water begrijpen:een neutrale uitleg
Dit is waarom:
* Dissociatie: Watermoleculen kunnen in zeer kleine mate dissociëren in waterstofionen (H+) en hydroxide-ionen (OH-).
* Evenwicht: Deze dissociatie bereikt een evenwicht, wat betekent dat de snelheid van voorwaartse en achterwaartse reacties gelijk is.
* Gelijke concentratie: Bij evenwicht is de concentratie van H+ en OH-ionen gelijk, wat ongeveer 10^-7 mol per liter is.
* pH-schaal: De pH-schaal is logaritmisch, waarbij pH 7 een neutrale oplossing vertegenwoordigt.
Daarom wordt gedestilleerd water (dm-water) als neutraal beschouwd met een pH van 7.
Belangrijke opmerking: In werkelijkheid kan gedestilleerd water lichtjes koolstofdioxide uit de lucht opnemen, waardoor het licht zuur kan worden (pH lager dan 7). Voor praktische doeleinden gaan we er echter vaak van uit dat gedestilleerd water een pH van 7 heeft.
 Onderzoekers ontwikkelen nieuwe methode om snel, betrouwbaar monitoren van sikkelcelziekte
Onderzoekers ontwikkelen nieuwe methode om snel, betrouwbaar monitoren van sikkelcelziekte Metaalkarakter van elementen:eigenschappen identificeren op het periodiek systeem
Metaalkarakter van elementen:eigenschappen identificeren op het periodiek systeem  Wat duidt op het relatieve aantal reactanten en producten in een chemische reactie?
Wat duidt op het relatieve aantal reactanten en producten in een chemische reactie?  Ontdekking van een ongebruikelijk eiwit
Ontdekking van een ongebruikelijk eiwit Wat is het mengsel van waterzout en modder?
Wat is het mengsel van waterzout en modder?
 Simulator voor boren op dieptes tot 5, 000 meter
Simulator voor boren op dieptes tot 5, 000 meter Een moddervulkaan barst al 10 jaar uit - en wetenschappers weten nog steeds niet wat de oorzaak is
Een moddervulkaan barst al 10 jaar uit - en wetenschappers weten nog steeds niet wat de oorzaak is Wat maken bomen als ze ademen?
Wat maken bomen als ze ademen?  Rioolafval in de magnetron kan het veilig maken om het als meststof voor gewassen te gebruiken
Rioolafval in de magnetron kan het veilig maken om het als meststof voor gewassen te gebruiken Wat is de relatie tussen de natuur en uw identiteit?
Wat is de relatie tussen de natuur en uw identiteit?
Hoofdlijnen
- Kanker beïnvloedt een mens alleen B de meeste eencellige organismen C Multicellulaire D -organismen?
- Waarom zou een wetenschapper een hogere versus lagere percentage agarose -oplossing gebruiken bij het bereiden van gel om DNA te scheiden?
- Wat is de naam van suikermolecuul in RNA?
- Drang om samen te voegen:begrijpen hoe cellen samensmelten
- Wetenschappers identificeren hoe de ontwikkeling van verschillende soorten dezelfde genen met verschillende kenmerken gebruikt
- Wat gebeurt er met het aantal witte bloedcellen tijdens een infectie?
- Een cel die in een oplossing wordt geplaatst, krimpt door het proces van osmose welke soort oplossing is buiten cel?
- Wat zou er met een organisme gebeuren als zijn celmembranen de meeste substantie permeabel werden?
- Hoeveel allelen voor één eigenschap worden normaal gevonden in het genotype van een organisme?
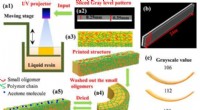
- 4D-printen van omkeerbare vormveranderende materialen met op licht gebaseerde grijswaardenpatronen
- Model voorspelt de neiging van polymere voedselverpakkingen om aromamoleculen uit hun inhoud te absorberen

- Transparant hout:het bouwmateriaal van de toekomst?

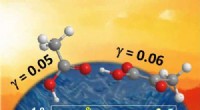
- Carbonzuren gedragen zich als superzuren op het wateroppervlak
- Dat is cool! Flash-bevroren foto's onthullen moleculaire wereld

 Wat is het belangrijkste kenmerk van levende organismen?
Wat is het belangrijkste kenmerk van levende organismen?  Hoeveel extra valentie -elektronen heeft chloor nodig om een volledige schaal te hebben?
Hoeveel extra valentie -elektronen heeft chloor nodig om een volledige schaal te hebben?  De EU waarschuwt dat het iPhones zal terugroepen als uit laboratoria blijkt dat ze defect zijn
De EU waarschuwt dat het iPhones zal terugroepen als uit laboratoria blijkt dat ze defect zijn  Opkomende landbouw en landschapsverstoringen bedreigen de doelstellingen van het klimaatakkoord van Parijs
Opkomende landbouw en landschapsverstoringen bedreigen de doelstellingen van het klimaatakkoord van Parijs Van welke natuurlijke hulpbronnen is fossiele energie afgeleid?
Van welke natuurlijke hulpbronnen is fossiele energie afgeleid?  Hoeveel atomen vormen een nucleotide?
Hoeveel atomen vormen een nucleotide?  Hoe veroorzaken bomen mechanische of fysieke verwering?
Hoe veroorzaken bomen mechanische of fysieke verwering?  Saturday Citations:Luisteren naar vogeldromen, qubits veiligstellen, onmogelijk biljart voorstellen
Saturday Citations:Luisteren naar vogeldromen, qubits veiligstellen, onmogelijk biljart voorstellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

