
Wetenschap
Zoutzuurstandaardisatie met behulp van Borax:een gedetailleerde gids
Standaardisatie van zoutzuur met borax
Inleiding:
Standaardisatie is het proces waarbij de precieze concentratie van een oplossing, zoals zoutzuur (HCl), wordt bepaald. Borax (natriumtetraboraatdecahydraat, Na₂B₄O₇·10H₂O) is een primaire standaard, wat betekent dat het een zeer zuivere, stabiele verbinding is die nauwkeurig kan worden gewogen en kan worden gebruikt om de concentratie van een andere oplossing te bepalen. Deze methode is gebaseerd op de reactie tussen borax en HCl, waarbij een zwak zuur (boorzuur) en een zout (natriumchloride) ontstaat.
Procedure:
1. Bereiding van Borax-oplossing:
- Weeg nauwkeurig ongeveer 2,0 g borax (Na₂B₄O₇·10H₂O) af en los dit op in ongeveer 100 ml gedestilleerd water.
- Breng de oplossing kwantitatief over in een maatkolf van 250 ml en vul aan tot de maatstreep met gedestilleerd water.
- Bereken de exacte concentratie van de boraxoplossing (molariteit).
2. Titratie:
- Vul een buret met de te standaardiseren HCl-oplossing.
- Pipetteer 25,00 ml van de boraxoplossing in een erlenmeyer.
- Voeg een paar druppels van een geschikte indicator toe, zoals methyloranje of broomcresolgroen.
- Titreer de boraxoplossing met de HCl-oplossing tot het eindpunt is bereikt (de kleurverandering van de indicator).
- Noteer het gebruikte volume HCl.
- Herhaal de titratie nog minimaal twee keer om nauwkeurige resultaten te garanderen.
Berekeningen:
1. Reactie stoichiometrie:
De reactie tussen borax en HCl is:
Na₂B₄O₇·10H₂O + 2HCl → 4H₃BO₃ + 2NaCl + 5H₂O
Uit deze vergelijking kun je zien dat 1 mol borax reageert met 2 mol HCl.
2. HCl-concentratie berekenen:
- Bereken het gemiddelde volume HCl dat bij de titratie is gebruikt.
- Gebruik de volgende formule:
Molariteit van HCl =(Molariteit van borax x volume van borax x 2) / volume van HCl
Voorbeeld:
- Stel dat u 2,00 g borax hebt gebruikt om een oplossing van 250 ml te bereiden. De molaire massa van borax is 381,37 g/mol.
- De molariteit van de boraxoplossing is:2,00 g / 381,37 g/mol / 0,250 L =0,0210 M.
- U hebt 25,00 ml van de boraxoplossing getitreerd en gemiddeld 23,45 ml HCl gebruikt.
- De molariteit van de HCl-oplossing is:(0,0210 M × 25,00 ml × 2) / 23,45 ml =0,0447 M .
Veiligheidsmaatregelen:
- Draag altijd een geschikte veiligheidsbril en handschoenen bij het hanteren van chemicaliën.
- Werk in een goed geventileerde ruimte.
- Ga voorzichtig om met zoutzuur, aangezien het bijtend is.
- Gooi chemicaliën op de juiste manier weg.
Opmerking: Dit is een basisoverzicht van het standaardisatieproces. Specifieke instructies en veiligheidsmaatregelen kunnen variëren, afhankelijk van het beschikbare laboratorium en de beschikbare apparatuur. Het is essentieel om uw laboratoriumhandleiding of uw instructeur te raadplegen voor gedetailleerde procedures en veiligheidsrichtlijnen.
 Lokaal geteeld? Het hangt allemaal af van hoe je het definieert
Lokaal geteeld? Het hangt allemaal af van hoe je het definieert  Jongeren gaan de straat op voor het klimaat:wie zijn ze?
Jongeren gaan de straat op voor het klimaat:wie zijn ze? Hoe is ecologie gerelateerd aan andere disciplines?
Hoe is ecologie gerelateerd aan andere disciplines?  Hoe bladsnijdermieren een schimmeltuin cultiveren om planten af te breken, zou inzicht kunnen geven in toekomstige biobrandstoffen
Hoe bladsnijdermieren een schimmeltuin cultiveren om planten af te breken, zou inzicht kunnen geven in toekomstige biobrandstoffen  Dit huis is van mening dat wetenschap een bedreiging voor de mensheid is?
Dit huis is van mening dat wetenschap een bedreiging voor de mensheid is?
Hoofdlijnen
- Onderzoek met bacteriën brengt wetenschappers een stap dichter bij het maken van kunstmatige cellen met levensechte functionaliteit
- Moet mRNA in een lipidelaag worden gehuld om als vaccin te dienen?
- Onderzoekers ontdekken hoe dodelijke biofilms ontstaan
- Welk type microscopie is de negatieve vlek vergelijkbaar?
- Welke twee stoffen worden gemaakt in de kern en gaan naar cytoplasma?
- Wat zijn de verschillen tussen biologisch en fylogenetisch concept van morfologische soorten?
- Wat is een kopie van DNA die vroeger het synthesespecifieke eiwit richtte?
- Wat zou er gebeuren in een menselijk lichaam dat zijn chromosomen heeft verloren op het moment dat de cel verdeelt zoals ze doen voor reparatie en regeneratie?
- Hoe verschilt cytokinese in plantencellen van menselijke en dierlijke cellen?
- een slimmere, veiligere manier om corrosie te verslaan:Onderzoek toont aan dat een nieuwe corrosieremmer 10 keer effectiever is

- Zo mooi als een pauw:de edelsteen voor de volgende generatie slimme sensoren

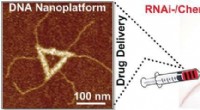
- DNA-origami vol krachtige antikankermiddelen
- Opzettelijke scheuren en rimpels bieden een goedkope optie voor medische screening

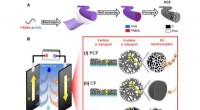
- Poreuze koolstofnanovezels vertonen uitzonderlijke capacitieve deïonisatie
 Wat is de vergelijking voor het verhitte jodium?
Wat is de vergelijking voor het verhitte jodium?  Eigenschappen van methaangas
Eigenschappen van methaangas Wanneer vulkanen metaal worden
Wanneer vulkanen metaal worden De temperatuur van de bodem verlagen:bodembedekkers beschermen de bodem tegen extreme temperaturen
De temperatuur van de bodem verlagen:bodembedekkers beschermen de bodem tegen extreme temperaturen Wat is de formule voor stikstofhydroxide en chloor?
Wat is de formule voor stikstofhydroxide en chloor?  Wanneer is de maan Rover uitgevonden?
Wanneer is de maan Rover uitgevonden?  Wat is de aard en vormen van elektriciteit?
Wat is de aard en vormen van elektriciteit?  Elektronische handschoen biedt menselijke eigenschappen voor gebruikers van prothesehanden
Elektronische handschoen biedt menselijke eigenschappen voor gebruikers van prothesehanden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

