
Wetenschap
Thermochemische vergelijkingen versus gebalanceerde chemische vergelijkingen:belangrijkste verschillen verklaard
Gebalanceerde chemische vergelijking:
* Focus: Toont de relatieve hoeveelheden reactanten en producten in een chemische reactie.
* Informatie:
* Chemische formules van reactanten en producten.
* Stoichiometrische coëfficiënten om de vergelijking in evenwicht te brengen (zorgen voor hetzelfde aantal van elk type atoom aan beide kanten).
* Voorbeeld: 2 H₂ + O₂ → 2 H₂O (Deze vergelijking vertelt ons dat 2 mol waterstof reageert met 1 mol zuurstof om 2 mol water te produceren).
Thermochemische vergelijking:
* Focus: Toont de enthalpieverandering (geabsorbeerde of afgegeven warmte) tijdens een chemische reactie.
* Informatie:
* Alle elementen van een uitgebalanceerde chemische vergelijking.
* Enthalpieverandering (ΔH) , wat een numerieke waarde is met een teken (+ of -) dat aangeeft of warmte wordt geabsorbeerd (endotherm, ΔH> 0) of vrijgegeven (exotherm, ΔH <0).
* Voorbeeld: 2 H₂ + O₂ → 2 H₂O ΔH =-571,6 kJ/mol (Deze vergelijking geeft aan dat 571,6 kJ warmte vrijkomt wanneer 2 mol waterstof reageert met 1 mol zuurstof om 2 mol water te vormen).
Samengevat:
* Alle thermochemische vergelijkingen zijn gebalanceerde chemische vergelijkingen, maar niet alle gebalanceerde chemische vergelijkingen zijn thermochemisch.
* Thermochemische vergelijkingen bieden aanvullende informatie over de energieveranderingen die bij de reactie betrokken zijn, waardoor ze uitgebreider worden.
Hoofdlijnen
- Onderzoekers ontdekken een manier om in eiwitten te kijken en te zien hoe ze in elkaar zitten
- Welke van de volgende hebben typische plantencellen dat dier niet?
- Wat is de belangrijkste functie van chromosoom?
- Welk type biochemisch molecuul is een enzym?
- Bacteriële structuren begrijpen:een uitgebreide gids
- Wat heeft sociaal -wetenschappelijke theorie?
- Wat zijn de doelstellingen van agarose?
- Wat gebeurt er met het pyrodruivenzuurmolecuul in de mitochondriale matrix?
- Hoe komen wetenschappers tegenwoordig uit of twee organismen gerelateerd zijn?
- Nieuwe studie onderzoekt de effectiviteit van nucleair afvalfilter op nanoschaal

- Techniek combineert op licht gebaseerde analytische methoden met microfluïdische monsterverwerking voor de diagnose van pathogenen

- Nieuwe moleculaire spier reageert op zichtbaar licht
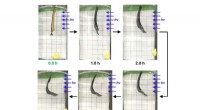
- Onderzoek naar de chemie van nucleaire explosies

- Team gebruikt 3D-printen om doorstroomelektroden voor elektrochemische reactoren te optimaliseren

 Rederijen kijken naar de toekomst
Rederijen kijken naar de toekomst Hoe zijn de 3 soorten zonnestraling zowel?
Hoe zijn de 3 soorten zonnestraling zowel?  Welke metalen krassen gemakkelijk?
Welke metalen krassen gemakkelijk?  Identificatie van het zout gevormd uit zoutzuur en natriumcarbonaat
Identificatie van het zout gevormd uit zoutzuur en natriumcarbonaat  Wat is de afstand van het sterrenbeeld Stier tot de aarde?
Wat is de afstand van het sterrenbeeld Stier tot de aarde?  Wat is het proces waarbij DNA wordt gedupliceerd?
Wat is het proces waarbij DNA wordt gedupliceerd?  Wat is de rol van de mens in zijn omgeving?
Wat is de rol van de mens in zijn omgeving?  Wanneer vindt zwaartekracht naar kinetische elektrische stroom plaats?
Wanneer vindt zwaartekracht naar kinetische elektrische stroom plaats?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


