
Wetenschap
Conversie van dichromaat naar chromaat:effect van de pH op chroomionen
Dichromaationen (Cr₂O₇²⁻) worden omgezet in chromaationen (CrO₄²⁻).
Hier is de chemische reactie:
Cr₂O₇²⁻ + H₂O ⇌ 2CrO₄²⁻ + 2H⁺
Deze reactie is een evenwichtsreactie en de evenwichtspositie verschuift naar rechts (ten gunste van chromaationen) wanneer de pH wordt verhoogd.
Dit is waarom:
* pH- en H⁺-concentratie: Naarmate de pH stijgt, neemt de concentratie H⁺-ionen af.
* Het principe van Le Chatelier: Het evenwicht verschuift om de stress te verlichten die wordt veroorzaakt door de afname van de H⁺-concentratie. Om dit te doen, verbruikt de reactie H⁺-ionen, waardoor het evenwicht naar rechts verschuift, waardoor meer chromaationen worden geproduceerd.
Resultaat:
* De oplossing zal van kleur veranderen. Dichromaationen zijn oranje, terwijl chromaationen geel zijn. Naarmate de pH stijgt, wordt de oplossing geler.
Andere belangrijke overwegingen:
* Evenwichtsconstante: De evenwichtsconstante voor deze reactie is ongeveer 3,2 x 10⁻¹⁴, wat aangeeft dat de reactie dichromaationen in zure oplossingen sterk bevoordeelt.
* Omkeerbaarheid: De reactie is omkeerbaar. Als de pH opnieuw wordt verlaagd, verschuift de reactie terug naar links, waarbij dichromaationen worden bevoordeeld.
Praktische toepassingen:
* Deze reactie wordt in de analytische chemie gebruikt om de concentratie van chromaat- of dichromaationen te bepalen.
*De kleurverandering kan ook als indicator bij titraties worden gebruikt.
Laat het me weten als je nog vragen hebt!
 Techniek verdubbelt conversie van CO2 naar plastic component
Techniek verdubbelt conversie van CO2 naar plastic component Wetenschappers verbeteren materialen voor reconstructieve en plastische chirurgie
Wetenschappers verbeteren materialen voor reconstructieve en plastische chirurgie  Hoe zijn de concentraties van waterstofionen en hydroxide gerelateerd in een waterige oplossing.
Hoe zijn de concentraties van waterstofionen en hydroxide gerelateerd in een waterige oplossing.  Proost! Wetenschappers zetten grote stap in de richting van het perfecte bierhoofd
Proost! Wetenschappers zetten grote stap in de richting van het perfecte bierhoofd Koperbromide en natriumsulfaat leveren wat op?
Koperbromide en natriumsulfaat leveren wat op?
 Wat zijn de stadia van de ontwikkeling van een orkaan?
Wat zijn de stadia van de ontwikkeling van een orkaan?  Weerbureau Macau in onderzoek wegens vertraagde tyfoonwaarschuwing
Weerbureau Macau in onderzoek wegens vertraagde tyfoonwaarschuwing Onderzoekers vinden een toename van 70 procent in atmosferische waterstof in de afgelopen 150 jaar
Onderzoekers vinden een toename van 70 procent in atmosferische waterstof in de afgelopen 150 jaar Waarom nemen we de tijd om de zaak te classificeren?
Waarom nemen we de tijd om de zaak te classificeren?  Oesterjagers verkennen rivieren op tekenen van schelpdierleven
Oesterjagers verkennen rivieren op tekenen van schelpdierleven
Hoofdlijnen
- Fruitvlieg helpt bij het ontsluiten van aanwijzingen over hoe organen, weefsel en kanker groeien
- Wat is een besmettelijk middel dat is samengesteld uit eenvoudig streng RNA zonder eiwitcomponent?
- Wat gebruiken biologen om vast te stellen of twee organismen van dezelfde soort zijn of niet?
- Wat zijn de overeenkomsten tussen bacteriën en plantencellen?
- Waar wordt Myelin gevonden en wat zijn functie?
- Wat betekent AI voor de Australische democratie? En wat kunnen we eraan doen?
- Nuclear DNA:Structure, Location &Function - A Comprehensive Guide
- Cellulaire ademhaling en het ademhalingssysteem:een vitale verbinding
- Vier hoofdelementen gevonden in een levend organisme?
- Nieuwe verbinding effectief tegen medicijnresistente pathogenen, kan leiden tot nieuwe antibiotica

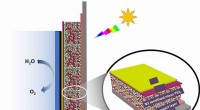
- Kleine titanium barrière stopt groot probleem in brandstofproducerende zonnecellen
- Nieuwe connector voor duurzame constructies op aarde en in de ruimte

- Voering van MOF-zakken om schadelijke gassen te detecteren

- Naar hoogwaardige mangaanoxidekatalysatoren met grote oppervlakten

 Wat zijn unieke chemische groepen die speciale eigenschappen verlenen aan een organisch molecuul dat wordt genoemd?
Wat zijn unieke chemische groepen die speciale eigenschappen verlenen aan een organisch molecuul dat wordt genoemd?  Verrassende ontdekking in de zoektocht naar energie-efficiënte informatieopslag
Verrassende ontdekking in de zoektocht naar energie-efficiënte informatieopslag Temperatuur, tijd en bosbessenwijn:onderzoekers onderzoeken de effecten van fermentatie op gezondheidsbevorderende stoffen
Temperatuur, tijd en bosbessenwijn:onderzoekers onderzoeken de effecten van fermentatie op gezondheidsbevorderende stoffen  Wat is de kleur van magma?
Wat is de kleur van magma?  Is de constante snelheid afhankelijk van richting?
Is de constante snelheid afhankelijk van richting?  Hoe het gemiddelde te berekenen in een waarschijnlijkheidsverdeling
Hoe het gemiddelde te berekenen in een waarschijnlijkheidsverdeling Organismen die genen van andere organismen bevatten, worden genoemd?
Organismen die genen van andere organismen bevatten, worden genoemd?  Wanneer de moleculen in een lichaam met verhoogde snelheid bewegen, wie zal er veranderen?
Wanneer de moleculen in een lichaam met verhoogde snelheid bewegen, wie zal er veranderen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

