
Wetenschap
Aminozuureigenschappen:hoe zijketens chemisch gedrag bepalen
Dit is waarom:
* De centrale structuur: Alle aminozuren delen een gemeenschappelijke structuur:een centraal koolstofatoom gebonden aan een waterstofatoom, een aminogroep (NH2), een carboxylgroep (COOH) en een zijketen (R-groep).
* De unieke R-groep: De zijketen (R-groep) is het enige deel dat varieert tussen de 20 aminozuren. Deze R-groep kan zijn:
* Hydrofoob (niet-polair): Deze groepen worden afgestoten door water en hebben de neiging samen te clusteren in eiwitstructuren. Voorbeelden zijn onder meer glycine, alanine en valine.
* Hydrofiel (polair): Deze groepen worden aangetrokken door water en bevinden zich vaak op het oppervlak van eiwitten. Voorbeelden hiervan zijn serine, threonine en asparagine.
* In rekening gebracht: Deze groepen kunnen positief of negatief geladen zijn en spelen een belangrijke rol in de eiwitfunctie. Voorbeelden hiervan zijn lysine, arginine en glutaminezuur.
* Impact op eigendommen: De chemische en fysische eigenschappen van elk aminozuur worden bepaald door zijn specifieke R-groep. Dit omvat:
* Grootte en vorm: R-groepen variëren in grootte, vorm en flexibiliteit en beïnvloeden de manier waarop aminozuren met elkaar en met andere moleculen interageren.
* Kosten: Geladen R-groepen dragen bij aan de algehele lading van een eiwit en beïnvloeden de interacties met andere moleculen.
* Reactiviteit: R-groepen kunnen deelnemen aan chemische reacties en de katalytische activiteit of bindingseigenschappen van het eiwit beïnvloeden.
Daarom is de diversiteit van R-groepen onder de 20 aminozuren de sleutelfactor die verantwoordelijk is voor het brede scala aan chemische en fysische eigenschappen die in eiwitten worden waargenomen.
 Fluorchloor en broom hebben allemaal zeven valentie -elektronen welk element heeft de grootste atoomradius?
Fluorchloor en broom hebben allemaal zeven valentie -elektronen welk element heeft de grootste atoomradius?  Wat zijn de producten van dubbele vervangingsreactie tussen kaliumchloride en zilveracetaat?
Wat zijn de producten van dubbele vervangingsreactie tussen kaliumchloride en zilveracetaat?  Nieuw bioremediatiemateriaal kan chemicaliën voor altijd reinigen
Nieuw bioremediatiemateriaal kan chemicaliën voor altijd reinigen Wat is de chemische samenstelling van ontschuimer?
Wat is de chemische samenstelling van ontschuimer?  Wat is de oorsprong van naam waterstof?
Wat is de oorsprong van naam waterstof?
 Wat is het onroerend goed dat verwijst naar manier waarop licht van een mineraal stuitert?
Wat is het onroerend goed dat verwijst naar manier waarop licht van een mineraal stuitert?  Video:CO2-uitstoot prijzen
Video:CO2-uitstoot prijzen Nieuwe studie toont aan dat bosbranden in Victoria in omvang en frequentie toenemen
Nieuwe studie toont aan dat bosbranden in Victoria in omvang en frequentie toenemen Hoe lang is 's werelds hoogste levende boom?
Hoe lang is 's werelds hoogste levende boom?  Satellietonderzoek toont aan dat de kusthotspots in Californië zinken
Satellietonderzoek toont aan dat de kusthotspots in Californië zinken
Hoofdlijnen
- Waarom is controle belangrijk in biologisch onderzoek?
- Wat is de wetenschappelijke betekenis van Ineria?
- Wat planten nodig hebben om droogte te weerstaan
- Wat zijn twee component van het endocrien systeem?
- Uitleg:Wat is antimaterie?
- Wat doet de centriole van een cel?
- Ziekten begrijpen:oorzaken, typen en belangrijkste kenmerken
- Hoe ver ben je van de boom gevallen? Wetenschappers schatten de mutatiesnelheid van chimpanseeouders tot hun nakomelingen
- Hoe belangrijk is een wetenschapper zijn?
- De geur van gerecycled plastic opsporen

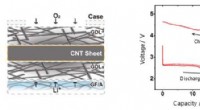
- Ontwikkeling van lithium-luchtbatterijen met ultrahoge capaciteit met behulp van CNT-blad-luchtelektroden
- Wereldprimeur voor het lezen van digitaal gecodeerde synthetische moleculen
- Wetenschappers slagen erin metalen glazen te verbeteren

- Hoe moleculen op oppervlakken zitten, stimuleert de overdracht van energie en elektronen

 Aluminiumoxide gevonden in een ultrahete Jupiter
Aluminiumoxide gevonden in een ultrahete Jupiter Hoe bereikt atomen een stabiele configuratie van edelgas?
Hoe bereikt atomen een stabiele configuratie van edelgas?  Wat gebeurt er met de zwaartekracht tussen twee objecten als de massa van één wordt verminderd?
Wat gebeurt er met de zwaartekracht tussen twee objecten als de massa van één wordt verminderd?  Wat is de meting van zowel snelheid als richting een object?
Wat is de meting van zowel snelheid als richting een object?  Waarom moet een cola-frisdrank worden gedecarboniseerd en een fosforzuurtitratie worden uitgevoerd?
Waarom moet een cola-frisdrank worden gedecarboniseerd en een fosforzuurtitratie worden uitgevoerd?  Hoe bouw je een 3D-geprinte deeltjesvanger met gratis CERN-schema's?
Hoe bouw je een 3D-geprinte deeltjesvanger met gratis CERN-schema's? Onderzoekers produceren 's werelds eerste programmeerbare nanoprocessor
Onderzoekers produceren 's werelds eerste programmeerbare nanoprocessor Ruimtewandelende astronauten upgraden station met nieuwe batterijen
Ruimtewandelende astronauten upgraden station met nieuwe batterijen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

