
Wetenschap
Wat zijn de producten van dubbele vervangingsreactie tussen kaliumchloride en zilveracetaat?
1. Identificeer de reactanten:
* Kaliumchloride (KCL)
* Zilveracetaat (Agc₂h₃o₂)
2. Begrijp dubbele vervangingsreacties:
In een dubbele vervangingsreactie veranderen de positieve en negatieve ionen van twee reactanten van partners. Dit kan worden weergegeven als:
AB + CD → AD + CB
3. Pas de regel toe op onze reactanten:
* KCL -> K⁺ + Cl⁻
* Agc₂h₃o₂ -> Ag⁺ + C₂h₃o₂⁻
4. Schakel de partners van:
* K⁺ combineert met c₂h₃o₂⁻ om kaliumacetaat te vormen (kc₂h₃o₂)
* Ag⁺ combineert met CL⁻ om zilveren chloride (AGCL) te vormen
5. Schrijf de gebalanceerde chemische vergelijking:
KCl (aq) + Agc₂h₃o₂ (aq) → kc₂h₃o₂ (aq) + agcl (s)
Belangrijke opmerking: Zilverchloride (AGCL) is onoplosbaar in water, dus het vormt een neerslag (een vaste stof die zich uit de oplossing vestigt).
Daarom zijn de producten van de dubbele vervangingsreactie tussen kaliumchloride en zilveracetaat kaliumacetaat (KC₂H₃O₂) en zilverchloride (AGCL).
 Oceanografen ontdekken de cruciale rol van het vermengen van zuurstof bij het in stand houden van de gezondheid van de diepzee
Oceanografen ontdekken de cruciale rol van het vermengen van zuurstof bij het in stand houden van de gezondheid van de diepzee  Vier soorten biodiversiteit
Vier soorten biodiversiteit  Als het om grondbewerking gaat, timing is belangrijk
Als het om grondbewerking gaat, timing is belangrijk Verwacht meer dodelijke hitte van klimaatverandering, studie zegt:
Verwacht meer dodelijke hitte van klimaatverandering, studie zegt: Na twintig jaar onderzoek naar de manier waarop ecosystemen koolstof absorberen, maken we ons zorgen over een instorting van het omslagpunt
Na twintig jaar onderzoek naar de manier waarop ecosystemen koolstof absorberen, maken we ons zorgen over een instorting van het omslagpunt
Hoofdlijnen
- Hoe de lengte van DNA-fragmenten te berekenen
- Hoe reproduceren planten zich als ze zaadloos zijn?
- Het verschil tussen genomisch DNA en plasmide-DNA
- Wat zijn de twee belangrijkste punten van osmose?
- Een methode voor het beschermen van de genetische identiteit Een populatie is onvermogen spermatozoa om Ova verschillende soorten te bemesten die dit noemt?
- Interferentie berekenen
- Het genennetwerk bepaalt hoeveel bloemen en vruchten planten zullen maken in het kritieke groeivenster
- Zijn de hersenen los van het skelet?
- Onderzoekers verkrijgen een momentopname die verduidelijkt hoe materialen cellen binnendringen
- Ingenieurs gebruiken warmtevrije technologie om metalen replica's te maken van een oppervlaktetextuur van rozen

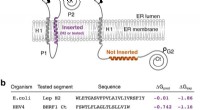
- Onderzoek toont de rol aan van intra-mebrane interacties bij de beheersing van celdood door virussen
- Nieuwe technologie zet afvalplastic in een uur om in vliegtuigbrandstof

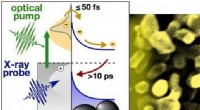
- Wetenschappers maken spontane snapshots van elektronen die licht oogsten op atomaire schaal
- Onderzoekers gebruiken neutronen om door las veroorzaakte stressverlichting in infrastructuur voor hernieuwbare energie te bestuderen

 Hoe cementmixers werken
Hoe cementmixers werken  Wat is een cederboom?
Wat is een cederboom?  Van stamcellen afgeleide levercellen geven nieuwe aanwijzingen voor ebola
Van stamcellen afgeleide levercellen geven nieuwe aanwijzingen voor ebola Welke stollingsgesteente heeft dezelfde chemische samenstelling als basalt maar een andere korrelgrootte?
Welke stollingsgesteente heeft dezelfde chemische samenstelling als basalt maar een andere korrelgrootte?  Wie was de vrouw van Apollo?
Wie was de vrouw van Apollo?  Welke voor- en nadelen zijn er om zonne -energiewarmtewater te gebruiken?
Welke voor- en nadelen zijn er om zonne -energiewarmtewater te gebruiken?  Wat is de betekenis van deze zee die haar boezem tot maan blijft?
Wat is de betekenis van deze zee die haar boezem tot maan blijft?  Gelaagde kamers openen een venster voor medicijnafgifte
Gelaagde kamers openen een venster voor medicijnafgifte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

