
Wetenschap
Alkaliteit uitgelegd:pH en neutralisatie begrijpen
Alkaliteit begrijpen:meer dan alleen maar 'basis'
Hoewel alkaliteit vaak wordt geassocieerd met ‘basisch zijn’ (een pH hoger dan 7 hebben), is het meer dan alleen dat. Hier is een overzicht van de alkaliteit:
1. De definitie:
Alkaliteit is het vermogen van een oplossing om zuren te neutraliseren . Het is een maatstaf voor hoeveel zuur een oplossing kan absorberen voordat er een significante verandering in de pH optreedt.
2. De chemie:
De alkaliteit wordt voornamelijk bepaald door de aanwezigheid van carbonaat- (CO3²⁻), bicarbonaat- (HCO3⁻) en hydroxide- (OH⁻)-ionen in de oplossing. Deze ionen fungeren als buffers en accepteren waterstofionen (H⁺) uit zuren, waardoor een dramatische daling van de pH wordt voorkomen.
3. Belang in verschillende systemen:
* Natuurlijke wateren: Alkaliteit is cruciaal voor het handhaven van de pH-balans van meren, rivieren en oceanen. Het helpt bij het reguleren van de zuurgraad van regenval, waardoor snelle veranderingen in de pH worden voorkomen die schadelijk kunnen zijn voor het waterleven.
* Zwembaden: Het handhaven van de juiste alkaliteit in zwembaden is belangrijk voor hygiëne en comfort. Het voorkomt corrosief water en houdt de pH binnen een gezond bereik.
* Bodem: De alkaliteit van de bodem beïnvloedt de plantengroei. Sommige planten gedijen in alkalische omstandigheden, terwijl andere het moeilijk hebben.
* Industriële processen: In veel industriële processen wordt alkaliteit gebruikt voor pH-controle en neutralisatiereacties.
4. Alkaliteit meten:
De alkaliteit wordt doorgaans gemeten in milligram per liter (mg/l) als calciumcarbonaat (CaCO3) .
5. Belangrijke punten om te onthouden:
* Alkaliteit is niet hetzelfde als pH: Alkaliteit beschrijft het *vermogen* om zuren te neutraliseren, terwijl de pH een maatstaf is voor de *werkelijke zuurgraad/basiciteit*.
* Hoge alkaliteit betekent niet noodzakelijkerwijs een hoge pH: Een oplossing met een hoge alkaliteit kan een relatief neutrale pH hebben als de buffercapaciteit niet volledig wordt benut.
* Alkaliteit is essentieel voor het handhaven van de pH-stabiliteit in verschillende systemen.
Het begrijpen van de alkaliteit is belangrijk voor verschillende toepassingen, van milieubeheer tot industriële processen. Door de alkaliteit onder controle te houden, kunnen we zorgen voor gezonde ecosystemen, veilige zwemomgevingen en efficiënte industriële activiteiten.
Hoofdlijnen
- Tijdens de menselijke ontwikkeling moet welk proces plaatsvinden voordat de celdeling kan plaatsvinden?
- Hoe werkt recombinant DNA?
- Welk organisme leeft op 235 Fahrenheit?
- Wat wordt gevormd in rood beenmerg en zijn het meest voorkomende type witte bloedcellen?
- Wat zijn oorzaken van evolutie en diversiteitsorganismen?
- Wat zijn de voorbeelden van eencellige organismen?
- Hoe jasmonaatsignalering wordt verbeterd onder fosforarme omstandigheden in de plantenfysiologie
- Welke wetenschappers kwamen op een ordelijke manier om levende wezens te classificeren?
- Populatie-ecologie: definitie, kenmerken, theorie en voorbeelden
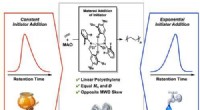
- Hoe biologies hardst werkende pigmenten en MOF's het klimaat kunnen redden

- Triangle 2 plastic containers kunnen een make-over voor het milieu ondergaan
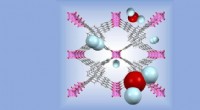
- Zeer modulaire materialen op metaal-organische basis vertonen een groot potentieel voor fotokatalytische waterstofproductie
- Serendipity verbreedt de mogelijkheden voor het maken van grafiet

- Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken
 Is de melkachtige manier een uitgestrekt spiraalvormige sterrenstelsel?
Is de melkachtige manier een uitgestrekt spiraalvormige sterrenstelsel?  Koolstofnanobuisjes ingebed in bladeren detecteren chemische signalen die worden geproduceerd wanneer een plant wordt beschadigd
Koolstofnanobuisjes ingebed in bladeren detecteren chemische signalen die worden geproduceerd wanneer een plant wordt beschadigd Maleisië redt 140 schubdieren van vermoedelijke smokkelaars
Maleisië redt 140 schubdieren van vermoedelijke smokkelaars Wat drijft de verspreiding van de zeebodem? De dynamiek van tektonische platen begrijpen
Wat drijft de verspreiding van de zeebodem? De dynamiek van tektonische platen begrijpen  Hoe u uw gazon het hele jaar door natuurvriendelijk kunt maken:tips van een ecoloog
Hoe u uw gazon het hele jaar door natuurvriendelijk kunt maken:tips van een ecoloog  Wat is zeer radioactief met kernenergie?
Wat is zeer radioactief met kernenergie?  Kunsthuid creëert eerste prikkelbare apparaten
Kunsthuid creëert eerste prikkelbare apparaten Klimaatverandering zal miljoenen mensen verdrijven. Waar zullen ze heen gaan?
Klimaatverandering zal miljoenen mensen verdrijven. Waar zullen ze heen gaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


