
Wetenschap
De oplosmiddeleigenschappen van water begrijpen:ionen oplossen
* Polariteit: Watermoleculen zijn gebogen, waarbij het zuurstofatoom een gedeeltelijke negatieve lading heeft en de waterstofatomen een gedeeltelijke positieve lading hebben. Hierdoor ontstaat een dipoolmoment, waardoor water een polair molecuul wordt.
* Waterstofbinding: De gedeeltelijke positieve ladingen op de waterstofatomen van watermoleculen kunnen sterke waterstofbruggen vormen met de negatieve ionen. Op dezelfde manier kan de gedeeltelijke negatieve lading op het zuurstofatoom interageren met positieve ionen.
* Oplossing: Wanneer een ionische verbinding in water wordt opgelost, omringen de polaire watermoleculen de individuele ionen, waardoor ze effectief van elkaar worden gescheiden. De positieve uiteinden van watermoleculen omringen de negatieve ionen, en omgekeerd. Dit proces wordt solvatie genoemd .
Dit is de reden waarom deze eigenschappen water tot een goed oplosmiddel voor ionen maken:
* Aantrekkingskrachten: De sterke elektrostatische aantrekkingskracht tussen de polaire watermoleculen en de ionen overwint de krachten die de ionische verbinding bij elkaar houden.
* Verspreiding: Het solvatatieproces verspreidt de ionen effectief door het water, waardoor wordt voorkomen dat ze zich opnieuw combineren en opnieuw een vaste stof vormen.
Samengevat: De polariteit van water en het vermogen om waterstofbruggen te vormen, zorgen ervoor dat het ionen kan omringen en isoleren, waardoor het een uitstekend oplosmiddel is voor ionische verbindingen.
 Er zijn watermoleculen voor nodig om dezelfde ruimte te vullen als ze in de vorm van ijs zijn als vergeleken vloeibaar water?
Er zijn watermoleculen voor nodig om dezelfde ruimte te vullen als ze in de vorm van ijs zijn als vergeleken vloeibaar water?  Wat is de binding in diatomic fluormolecuul F2 geroepen en hoe nog meer hydroxide-ion oh- genaamd?
Wat is de binding in diatomic fluormolecuul F2 geroepen en hoe nog meer hydroxide-ion oh- genaamd?  Welke twee temperatuurschalen worden gebruikt in de chemie?
Welke twee temperatuurschalen worden gebruikt in de chemie?  Wat betekent het als u zegt dat water een polaire moleculen is?
Wat betekent het als u zegt dat water een polaire moleculen is?  Inzicht in pH 5,5:zuur of alkalisch? | [Uw merknaam]
Inzicht in pH 5,5:zuur of alkalisch? | [Uw merknaam]
 Voorspellingen verifiëren voor grote plotselinge opwarming in de stratosfeer
Voorspellingen verifiëren voor grote plotselinge opwarming in de stratosfeer Een diepe duik in een beter begrip van stikstofeffecten
Een diepe duik in een beter begrip van stikstofeffecten Welke gevolgen heeft de klimaatcrisis voor de Antarctische pelsrob?
Welke gevolgen heeft de klimaatcrisis voor de Antarctische pelsrob?  Spionagesatellieten uit het Koude Oorlog-tijdperk onthullen mogelijke effecten van klimaatverandering
Spionagesatellieten uit het Koude Oorlog-tijdperk onthullen mogelijke effecten van klimaatverandering Hoe zit het met bladverliezende bomen in de winter is niet waar?
Hoe zit het met bladverliezende bomen in de winter is niet waar?
Hoofdlijnen
- De verschillen tussen kokkels en sint-jakobsschelpen
- Wat bestaat uit cellen?
- Wat is een manier waarop planten zich voortplanten?
- Waarom spierveroudering versnelt na 50 jaar:inzichten en strategieën
- Teams van sperma zwemmen soepeler tegen de stroom in
- Kan natuurlijke selectie optreden in een individueel organisme?
- Wat is goed voor je slechte besmettelijke bacteriën
- Neemt Facebook eindelijk anonimiteit serieus?
- De structuur van cellen die zijn grenzen leveren, wordt genoemd?
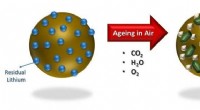
- De ultieme voorwaarden om het meeste uit nikkelrijke batterijen te halen
- Wetenschappers ontdekken gemeenschappelijke blauwdruk voor eiwitantibiotica

- Veelvoorkomende valkuilen bij het gebruik van pH-strips:hoe u fouten kunt voorkomen

- Wetenschappers testen nieuw materiaal voor neurocomputers

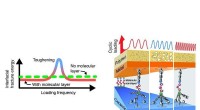
- Nanoglue kan composieten meerdere malen sterker maken tijdens dynamische belasting
 Uit onderzoek blijkt hoe RNA-‘junk’ onze genen controleert
Uit onderzoek blijkt hoe RNA-‘junk’ onze genen controleert  Een vlucht langs de bloed-hersenbarrière maken voor medicijnafgifte
Een vlucht langs de bloed-hersenbarrière maken voor medicijnafgifte Nieuwe synthesestrategie versnelt identificatie van eenvoudigere versies van een natuurlijk product
Nieuwe synthesestrategie versnelt identificatie van eenvoudigere versies van een natuurlijk product Energiegerelateerde organellen:hoe mitochondriën en chloroplasten het leven versterken
Energiegerelateerde organellen:hoe mitochondriën en chloroplasten het leven versterken  Hoe beïnvloedt warmte -energie de verdamping?
Hoe beïnvloedt warmte -energie de verdamping?  De zon is de heetste ster in het universum.
De zon is de heetste ster in het universum.  Canada overweegt belasting op internetreuzen
Canada overweegt belasting op internetreuzen Wereld gewaarschuwd:verander nu of breng voedsel en klimaat in gevaar
Wereld gewaarschuwd:verander nu of breng voedsel en klimaat in gevaar
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

