
Wetenschap
Welke lading voor hydrofobe aminozuren hebben bij PH6?
Dit is waarom:
* Hydrofobiciteit: Hydrofobe aminozuren hebben zijketens die zich niet aangetrokken voelen tot water. Ze zijn liever in het interieur van eiwitten, weg van de waterige omgeving.
* Niet-polaire zijketens: Hun zijketens hebben geen groepen die gemakkelijk protonen (H+ ionen) winnen of verliezen om opgeladen te worden.
* pH en ionisatie: De pH van een oplossing beïnvloedt de ionisatietoestand van aminozuren. Bij pH 6 wordt de carboxylgroep (COOH) van aminozuren in het algemeen gedeprotoneerd (COO-) en wordt de aminogroep (NH2) in het algemeen geprotoneerd (NH3+). Deze ladingen bevinden zich echter op de ruggengraat van het aminozuur, niet op de zijketens van hydrofobe aminozuren.
Voorbeelden van hydrofobe aminozuren:
* Alanine (Ala, A)
* Valine (Val, V)
* Leucine (Leu, L)
* Isoleucine (ile, i)
* Proline (Pro, P)
* Fenylalanine (Phe, F)
* Tryptophan (TRP, W)
* Methionine (Met, M)
Opmerking: Hoewel deze aminozuren typisch niet zijn opgeladen bij pH 6, kunnen er enkele kleine variaties zijn, afhankelijk van de specifieke eiwitomgeving. Hun primaire kenmerk is echter hun ontbreken van een belangrijke lading.
 Team ontwikkelt gasdetectietechnologie die een revolutie teweeg kan brengen in de milieu- en medische diagnostiek
Team ontwikkelt gasdetectietechnologie die een revolutie teweeg kan brengen in de milieu- en medische diagnostiek Marihuana hoe werkt
Marihuana hoe werkt  Wat is de oxidatietoestand van aluminium in fluoride?
Wat is de oxidatietoestand van aluminium in fluoride?  Activiteit van brandstofcelkatalysatoren verdubbeld
Activiteit van brandstofcelkatalysatoren verdubbeld Een onbekende carbonylverbinding testte positief wanneer gemengd met chrominezuuroplossing het liet ook resultaten zien in de jodoform -testtrekkingsstrutuur van deze verbinding?
Een onbekende carbonylverbinding testte positief wanneer gemengd met chrominezuuroplossing het liet ook resultaten zien in de jodoform -testtrekkingsstrutuur van deze verbinding?
 Kan een verenigd pad voor ontwikkeling en behoud tot een betere toekomst leiden?
Kan een verenigd pad voor ontwikkeling en behoud tot een betere toekomst leiden?  Drugsvervuiling concentreert zich in streambugs, gaat over op roofdieren in het water en op het land
Drugsvervuiling concentreert zich in streambugs, gaat over op roofdieren in het water en op het land Nieuw onderzoek laat zien waarom kinderen in armoede belanden
Nieuw onderzoek laat zien waarom kinderen in armoede belanden  Common North Dakota Spiders
Common North Dakota Spiders  Vier dingen om te weten over het nieuwste IPCC-klimaatrapport
Vier dingen om te weten over het nieuwste IPCC-klimaatrapport
Hoofdlijnen
- Draagt de mannelijke of vrouwelijke gameet meer chromosomen bij aan de bevruchte eicel?
- Hoe ziet een schildpadcel eruit?
- Wat zijn de kenmerken van de biosfeer?
- Welk deel ondersteunt een plantencel?
- Welke functies dienen displays en rituelen op dieren?
- Droogte decimeert de belangrijkste katoenoogst in Texas
- Foster-kikkervisjes triggeren het ouderlijk instinct bij gifkikkers
- Indonesische smokkelaars stopten exotische vogels in pijpen:politie
- Wat is de functie van mitose in uw lichaam?
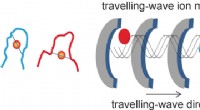
- Travelling-wave ion mobility massaspectrometrie verheldert structuren van gouden vingers
- Nieuw, volledig biologisch afbreekbaar cellulosemembraan blijkt effectief bij olie-waterscheiding

- Van oude spijkerbroek naar nieuw T-shirt

- Methode om microfluïdische elektrochemische technologieën toe te passen op redox-neutrale reacties met één elektronoverdracht
- Gereconstitueerde zijde kan meerdere keren sterker zijn dan de natuurlijke vezel en in verschillende vormen worden gemaakt

 Onderzoekers rapporteren tandeloze bevindingen in odontode-dragende meervalstudie
Onderzoekers rapporteren tandeloze bevindingen in odontode-dragende meervalstudie Kameleons inspireren nieuwe meerkleurige 3D-printtechnologie
Kameleons inspireren nieuwe meerkleurige 3D-printtechnologie  Nieuw, zeer gedetailleerde details over klimaatverandering voor Duitse provincies
Nieuw, zeer gedetailleerde details over klimaatverandering voor Duitse provincies Wat zijn condensatie -kernen?
Wat zijn condensatie -kernen?  Wat betekent zout sneller in heet water?
Wat betekent zout sneller in heet water?  Hoe helpen plaattektoniek de aanwezigheid van unieke diersoorten op continenten zoals Australië te verklaren?
Hoe helpen plaattektoniek de aanwezigheid van unieke diersoorten op continenten zoals Australië te verklaren?  In Arizona is dit natuurlijke monument van kleurrijke rots 4000 voet diep?
In Arizona is dit natuurlijke monument van kleurrijke rots 4000 voet diep?  Hoe werken drukknopschakelaars in een elektrisch circuit?
Hoe werken drukknopschakelaars in een elektrisch circuit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

