
Wetenschap
Verschil tussen organische en anorganische stoffen?
Hier is een uitsplitsing:
Organische stoffen:
* Bevat koolstof (C) als het primaire element. Ze bevatten vaak andere elementen zoals waterstof (H), zuurstof (O), stikstof (N), fosfor (P) en zwavel (S).
* hebben complexe structuren: Ze vormen lange ketens, ringen en vertakte structuren, vaak met functionele groepen bevestigd.
* meestal geassocieerd met levende organismen: Ze worden gevonden in planten, dieren en micro -organismen.
* Voorbeelden: Koolhydraten, eiwitten, lipiden, nucleïnezuren, kunststoffen, aardolieproducten.
* Meestal ontvlambaar: Ze verbranden gemakkelijk en geven energie vrij.
anorganische stoffen:
* Bevat geen koolstof (C) als het primaire element. Uitzonderingen zijn onder meer koolstofdioxide (CO2), carbonaten en bicarbonaten.
* hebben eenvoudiger structuren: Ze vormen vaak ionische of covalente bindingen, waardoor eenvoudige moleculen of kristallijne structuren ontstaan.
* gevonden in niet-levende materie: Ze zijn te vinden in rotsen, mineralen, lucht en water.
* Voorbeelden: Water (H2O), zout (NaCl), zand (SiO2), metalen (ijzer, goud, zilver), glas.
* Over het algemeen niet-brandbaar: Ze branden niet gemakkelijk.
Belangrijke punten om te onthouden:
* Dit onderscheid is niet absoluut. Sommige verbindingen bevatten zowel koolstof als andere elementen en hebben kenmerken van zowel organische als anorganische stoffen.
* De aanwezigheid van koolstof is de meest voorkomende bepalende factor, maar niet de enige.
* Organische chemie is een enorm veld gewijd aan de studie van koolstofhoudende verbindingen en hun reacties.
Hier is een nuttige analogie:
Denk aan een huis gebouwd van LEGO -bakstenen. De Lego -stenen zijn als de koolstofatomen en het huis is het complexe organische molecuul. Anorganische stoffen zijn als de individuele bouwstenen die het huis vormen, maar ze vormen niet de complexe structuren.
Hoofdlijnen
- Wat zijn biomedische wetenschappen?
- Red Tit-toxine stuurde hen naar het ziekenhuis. Kijk wat er gebeurde met een paar Florida-schildpadden
- Wat is een reactie van een organismen op een stimulus die wordt genoemd?
- Wat is een basiseenheid van structuur en functie gevonden in alle Ilvung -dingen?
- Wetenschappers proberen oude slachtmethoden na te bootsen en leren hoe Neanderthalers vogels aten
- Wat zijn de verschillende vormen van wetenschappelijke kennis?
- Hoe voorspelbaar is evolutie?
- Wat is de volgorde van base os agctcag op tegenover Strand?
- Auto-immuniteit kan verklaren waarom een belangrijk immuunsysteem bij veel bacteriën ontbreekt
- Onderzoekers ontwikkelen een rekrek voor cellen

- Chemokinereceptor CX3CR1-structuren onthullen mechanisme van cholesterolregulatie bij activering
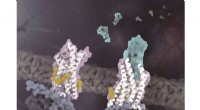
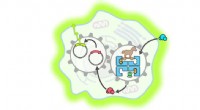
- Kunstmatig enzym kan een gen-switch activeren
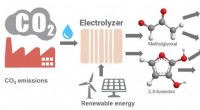
- Hoe klimaatveranderende koolstofdioxide om te zetten in plastic en andere producten?
- Kader voor het bestuderen van ozonniveaus op realistische binnenoppervlakken

 Wat is thermische en elektrische geleidingen?
Wat is thermische en elektrische geleidingen?  Vreemd maar waar: kietelen van je oor kan veroudering vertragen
Vreemd maar waar: kietelen van je oor kan veroudering vertragen Continue activiteit van kleine aardbevingen doet bergen groeien
Continue activiteit van kleine aardbevingen doet bergen groeien Wat zijn alle dingen die ons omringen, inclusief luchtwaterland en bomen?
Wat zijn alle dingen die ons omringen, inclusief luchtwaterland en bomen?  Wanneer is de gemiddelde versnelling gelijk aan onmiddellijke snelheid?
Wanneer is de gemiddelde versnelling gelijk aan onmiddellijke snelheid?  Zit er sneeuw in die boom? Burgerwetenschap helpt bij het ontrafelen van het sneeuweffect op de watervoorziening in de zomer
Zit er sneeuw in die boom? Burgerwetenschap helpt bij het ontrafelen van het sneeuweffect op de watervoorziening in de zomer Hoe kun je zien welke manier naar het noorden is in een bos?
Hoe kun je zien welke manier naar het noorden is in een bos?  Hoe de Melkweg werkt
Hoe de Melkweg werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


