
Wetenschap
Hoe pH verandert met temperatuurverandering?
1. De stof zelf:
* zuren: Voor de meeste zuren neemt pH af met toenemende temperatuur. Dit komt omdat het evenwicht tussen het zuur en zijn conjugaatbasis verschuift naar de conjugaatbasis, wat leidt tot een toename van H+ -ionen en een afname van de pH.
* Bases: Voor de meeste basen neemt pH toe met toenemende temperatuur. Dit komt omdat het evenwicht tussen de basis en zijn conjugaatzuur verschuift naar het conjugaatzuur, wat leidt tot een afname van OH-ionen en een toename van de pH.
2. Het oplosmiddel:
* Water: De autoionisatie van water is een endotherme proces, wat betekent dat het warmte absorbeert. Naarmate de temperatuur toeneemt, verschuift het evenwicht om de productie van meer H+ en OH-ionen te bevorderen, wat leidt tot een afname van de pH .
3. De aanwezigheid van andere stoffen:
* buffers: Buffers weerstaan veranderingen in pH, maar hun effectiviteit kan worden beïnvloed door temperatuur. De evenwichtsconstante van het buffersysteem verandert met temperatuur, die de pH kan beïnvloeden.
* opgeloste gassen: De oplosbaarheid van gassen in water neemt af met toenemende temperatuur. Dit kan de pH van oplossingen die opgeloste gassen bevatten, beïnvloeden, zoals CO2, die koolzuur in oplossing vormen.
Samenvattend:
* voor de meeste zuren neemt de pH af met toenemende temperatuur.
* voor de meeste basen neemt de pH toe met toenemende temperatuur.
* De pH van zuiver water neemt af met toenemende temperatuur.
* Het effect van temperatuur op de pH kan complex zijn en hangt af van de specifieke stof en omstandigheden.
Belangrijke opmerking: De exacte relatie tussen pH en temperatuur is specifiek voor elke stof en oplossing. Het is cruciaal om relevante gegevens te raadplegen of experimenten uit te voeren om het precieze effect van de temperatuur op de pH voor een bepaald systeem te bepalen.
 Hoogste zeewatertemperatuur ooit gemeten bij Scripps Pier
Hoogste zeewatertemperatuur ooit gemeten bij Scripps Pier Wat betekent aanpassing in plantenwetenschap?
Wat betekent aanpassing in plantenwetenschap?  Toename van extreme neerslag in het noordoosten veroorzaakt door Atlantische variabiliteit en klimaatverandering
Toename van extreme neerslag in het noordoosten veroorzaakt door Atlantische variabiliteit en klimaatverandering Oceanen:ze vervuilen, ze betalen
Oceanen:ze vervuilen, ze betalen Mensen zijn bereid meer te betalen om Everglades te beschermen als ze deze twee dingen weten
Mensen zijn bereid meer te betalen om Everglades te beschermen als ze deze twee dingen weten
Hoofdlijnen
- Is ze zwanger? DC Zoo zegt dat de hormonen van panda stijgen
- Waarom doe je onderzoek?
- Naarmate het klimaat warmer wordt, muizen morph
- Hier ziet u hoe virussen het immuunsysteem inactiveren en kanker veroorzaken
- Hoe definieer je haat?
- Hoe worden nieuwe cellen geproduceerd?
- Wat is het model van mogelijke voedings- of energieoverdrachtsrelaties tussen meerdere organismen in een gemeenschap?
- Hoeveel takken heeft de biologie?
- Wat groeien kankercellen en vervangen gezond dat dit wordt genoemd?
- Splashdown:Supersonische koudmetaalverbinding in 3D

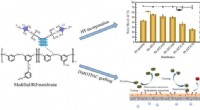
- Nieuwe technologie om de hoge permselectiviteit en anti-biofouling eigenschappen van RO-membranen te verbeteren
- Commercieel relevante op bismut gebaseerde dunnefilmverwerking

- Onderzoeksteams ontdekken buitengewone eigenschappen van strontiumniobaat

- Stabiele perovskiet-LED's een stap dichterbij

 Wat kan nog meer veranderen in een vloeistof van vaste tot vloeistof?
Wat kan nog meer veranderen in een vloeistof van vaste tot vloeistof?  Verloren of uitgestorven? Uit onderzoek blijkt dat het bestaan van meer dan 500 diersoorten onzeker blijft
Verloren of uitgestorven? Uit onderzoek blijkt dat het bestaan van meer dan 500 diersoorten onzeker blijft  Een sterrenbeeld dat aan de oostelijke horizon bij zonsondergang is, is een maand later?
Een sterrenbeeld dat aan de oostelijke horizon bij zonsondergang is, is een maand later?  Welk bewijs is er dat waterstof in zoutzuur verschilt van water?
Welk bewijs is er dat waterstof in zoutzuur verschilt van water?  Welk type telescoop zou worden gebruikt om een dichte koude wolk in de ruimte te bestuderen?
Welk type telescoop zou worden gebruikt om een dichte koude wolk in de ruimte te bestuderen?  Dieren die in het tropische woud leven en die omnivoren zijn
Dieren die in het tropische woud leven en die omnivoren zijn Wat is 1,8 m gelijk aan inches?
Wat is 1,8 m gelijk aan inches?  Spreek wiskunde, niet coderen
Spreek wiskunde, niet coderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

