
Wetenschap
Het effect van substraatconcentratie op de snelheidsreactie H202 en catalase?
Het effect van substraatconcentratie op de reactiesnelheid van H2O2 en Catalase
De reactie tussen waterstofperoxide (H2O2) en catalase is een klassiek voorbeeld van enzymkinetiek. Catalase, een enzym gevonden in bijna alle levende organismen, katalyseert de ontleding van H2O2 in water (H2O) en zuurstof (O2).
Hier is hoe substraatconcentratie de reactiesnelheid beïnvloedt:
1. Initiële toename van de snelheid:
* Bij lage substraatconcentraties neemt de reactiesnelheid evenredig toe met toenemende H2O2 -concentratie. Dit komt omdat er meer substraatmoleculen beschikbaar zijn om te binden aan de actieve plaatsen van het catalase -enzym.
* Dit is de eerste-orde Kinetiekgebied, waar de reactiesnelheid recht evenredig is met de substraatconcentratie.
2. Verzadigingspunt:
* Naarmate de substraatconcentratie verder toeneemt, is de reactiesnelheid uiteindelijk plateaus. Dit komt omdat alle actieve plaatsen van het catalase -enzym verzadigd raken met H2O2 -moleculen.
* Zelfs als meer H2O2 wordt toegevoegd, zal de reactiesnelheid niet toenemen omdat het enzym niet meer substraat kan binden.
3. Zero-orde kinetiek:
* Bij zeer hoge substraatconcentraties wordt de reactiesnelheid onafhankelijk van de substraatconcentratie. Dit komt omdat het enzym op maximale capaciteit werkt en het toevoegen van meer substraat de snelheid niet zal verhogen.
* Dit is de nulorder Kinetiekregio.
factoren die het verzadigingspunt beïnvloeden:
* Enzymconcentratie: Een hogere enzymconcentratie zal het verzadigingspunt verhogen, omdat er actievere locaties beschikbaar zullen zijn voor binding.
* Temperatuur: Optimale temperatuur verhoogt de reactiesnelheid, maar kan ook het enzym ontkennen. Hogere temperaturen kunnen het verzadigingspunt verschuiven naar hogere substraatconcentraties.
* pH: Elk enzym heeft een optimale pH voor activiteit. Afwijken van de optimale pH kan de efficiëntie van het enzym verminderen en het verzadigingspunt verschuiven.
grafisch:
De relatie tussen substraatconcentratie en reactiesnelheid kan worden gevisualiseerd met een grafiek:
* x-as: Substraatconcentratie (H2O2)
* y-as: Reactiesnelheid (hoeveelheid product gevormd per tijdseenheid)
De grafiek zal een karakteristieke curve vertonen, aanvankelijk steil oprijst en vervolgens op het verzadigingspunt plegen.
Belang:
Inzicht in het effect van substraatconcentratie op de reactiesnelheid is cruciaal voor:
* Inzicht in enzymkinetiek: Deze kennis helpt ons enzymfunctie, mechanisme en regulatie te bestuderen.
* Enzymatische reacties optimaliseren: Door de substraatconcentratie aan te passen, kunnen we de reactiesnelheid voor specifieke toepassingen optimaliseren.
* Modellering van biologische processen: Deze kennis is cruciaal voor het begrijpen van het gedrag van enzymen in levende organismen.
Samenvattend neemt de reactiesnelheid tussen H2O2 en catalase aanvankelijk evenredig toe met toenemende substraatconcentratie, vervolgens plateaus op het verzadigingspunt, en worden uiteindelijk onafhankelijk van de substraatconcentratie bij zeer hoge concentraties. Deze relatie is cruciaal voor het begrijpen van enzymkinetiek en het optimaliseren van enzymatische reacties.
 Een hoge energiebinding in ATP wordt gevormd wanneer gehydrolzeerd naar ADP en één fosfaatgroep?
Een hoge energiebinding in ATP wordt gevormd wanneer gehydrolzeerd naar ADP en één fosfaatgroep?  Is zwavel hexafluoride een voorbeeld van polyatomisch?
Is zwavel hexafluoride een voorbeeld van polyatomisch?  Hoe een wetenschapsproject te doen op vingerafdrukken
Hoe een wetenschapsproject te doen op vingerafdrukken  Is zout een combinatie van 2 pure stoffen?
Is zout een combinatie van 2 pure stoffen?  Waarom veroorzaken moleculen in de lucht weerstand?
Waarom veroorzaken moleculen in de lucht weerstand?
 Storms Alpha en Beta genoemd naar Grieks alfabet, tweede keer ooit
Storms Alpha en Beta genoemd naar Grieks alfabet, tweede keer ooit Dit is ijs op Antarctica, stroomt in slow motion als water dat door stroomversnellingen stroomt
Dit is ijs op Antarctica, stroomt in slow motion als water dat door stroomversnellingen stroomt Campustuininitiatieven kunnen de volgende generatie milieuveranderaars helpen groeien
Campustuininitiatieven kunnen de volgende generatie milieuveranderaars helpen groeien  Welke observatie kan een wetenschapper maken over blad?
Welke observatie kan een wetenschapper maken over blad?  Greta Thunberg zegt dat het klimaatdebat langzaam verschuift
Greta Thunberg zegt dat het klimaatdebat langzaam verschuift
Hoofdlijnen
- Welke celstructuur is belangrijk bij homeostase?
- Waarom contractiele vacuolen van weinig waarde zijn voor één celorganismen die in de oceaan leven?
- Wat is de eerste barrière voor genenstroom in allopatrische speciatie?
- Hoe zorgwekkend is de verspreiding van de vogelgriep naar melkkoeien? Dit is wat experts zeggen
- Welke levensfunctie is primair betrokken bij de omzetting van in energie opgeslagen organische moleculen naar een vorm die direct bruikbaar is voor de cel?
- De ruggengraat van DNA bestaat uit?
- Water is belangrijk voor de interacties van biologische moleculen omdat?
- Wat wordt gebruikt om weefsels te bouwen en levensfuncties uit te voeren in veel organismen?
- Hoe dragen mensen bij aan zaadverspreiding?
- Video:Werken anti-rimpelcrèmes?

- Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak
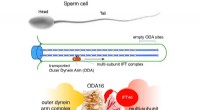
- Transport van moleculaire motoren naar trilhaartjes
- Met metaaloxide doordrenkte membranen kunnen een energiezuinig alternatief bieden voor chemische scheidingen

- Kaliumjacht op eiwitfabrieken

 Zijn de categorieën dier als plant of schimmel nuttig bij het classificeren van protisten?
Zijn de categorieën dier als plant of schimmel nuttig bij het classificeren van protisten?  Buitenschoolse activiteiten voor kinderen in China zijn beperkt praktisch
Buitenschoolse activiteiten voor kinderen in China zijn beperkt praktisch Hoe is wetenschapper op zoek naar een buitenaards leven?
Hoe is wetenschapper op zoek naar een buitenaards leven?  De doorbraak van onderzoekers op het gebied van thermisch transport zou nieuwe koelstrategieën mogelijk kunnen maken
De doorbraak van onderzoekers op het gebied van thermisch transport zou nieuwe koelstrategieën mogelijk kunnen maken  Een probioticum voor onze longen? Nieuw onderzoek roept vragen op over de toekomst van de behandeling van COVID-19
Een probioticum voor onze longen? Nieuw onderzoek roept vragen op over de toekomst van de behandeling van COVID-19  Wat is NO2 H2O?
Wat is NO2 H2O?  Wat is de pH-waarde van baking soda?
Wat is de pH-waarde van baking soda?  Hoe produceerde het Thales -experiment statische elektriciteit?
Hoe produceerde het Thales -experiment statische elektriciteit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

