
Wetenschap
Een organische verbinding die niet oplosbaar is in water?
koolwaterstoffen:
* hexaan (C6H14): Een gemeenschappelijk oplosmiddel dat in laboratoria wordt gebruikt, is hexaan een niet -polair molecuul en mengt dus niet met water.
* benzeen (C6H6): Een cyclische koolwaterstof, benzeen is ook niet -polair en onoplosbaar in water.
* toluen (C7H8): Een ander veel voorkomend oplosmiddel, tolueen is een niet -polaire vloeistof.
vetten en oliën:
* olijfolie (mengsel van triglyceriden): Oliën zijn samengesteld uit lange ketens van vetzuren, die niet -polair zijn en daarom onoplosbaar zijn in water.
* boter (mengsel van vetten en water): Hoewel boter wat water bevat, is de meerderheid dik, waardoor het meestal onoplosbaar is.
Andere voorbeelden:
* naftaleen (C10H8): Een vaste koolwaterstof, naftaleen, is het belangrijkste onderdeel van mottenballen.
* chloorbenzeen (C6H5CL): Deze verbinding heeft een niet-polaire benzeenring en een enigszins polaire koolstof-chloorbinding, waardoor het onoplosbaar is in water.
Waarom zijn deze verbindingen onoplosbaar in water?
De algemene vuistregel is "zoals oplost zoals". Water is een polair molecuul, wat betekent dat het een positief en negatief einde heeft. Niet -polaire moleculen zoals koolwaterstoffen hebben geen ladingscheiding en worden daarom niet aangetrokken tot watermoleculen. Dit gebrek aan aantrekkingskracht voorkomt dat ze oplossen.
Laat het me weten als je een van deze verbindingen in meer detail wilt verkennen!
 Klimaatverandering vermenigvuldigt schadelijke mariene hittegolven (update)
Klimaatverandering vermenigvuldigt schadelijke mariene hittegolven (update) Dodelijke olieramp in Indonesië veroorzaakt door gesprongen leiding:bedrijf
Dodelijke olieramp in Indonesië veroorzaakt door gesprongen leiding:bedrijf Wat zijn daar enkele variëteiten -bomen?
Wat zijn daar enkele variëteiten -bomen?  De vervuilde Po-vallei in Italië snakt naar frisse lucht
De vervuilde Po-vallei in Italië snakt naar frisse lucht Bosbomen in het zuidwesten zullen in de 21e eeuw veel langzamer groeien
Bosbomen in het zuidwesten zullen in de 21e eeuw veel langzamer groeien
Hoofdlijnen
- Wat zijn de dieren en schimmels die afhankelijk zijn van autotrofen voor hun voedselergie?
- Wat is een observatie bewijst dat cel eukaryote?
- Hoe worden organische systemen geactiveerd of gestimuleerd en ontwikkeld door activiteit?
- Bijen en vlinders gaan achteruit in westelijk en zuidelijk Noord-Amerika
- In welk koninkrijk is sporen?
- Produceert het lymfestelsel hormonen en enzymen?
- Zijn linkshandigen beter in sport?
- Welk weefsel covrs en lijnen vele delen van het lichaam?
- Welke organel is verantwoordelijk voor het vasthouden van chemicaliën die nodig zijn om de spijsvertering in een dierlijke cel te houden?
- Waterstofbindingen voor het eerst direct gedetecteerd

- Plastic web printen om de gsm-schermen van de toekomst te beschermen

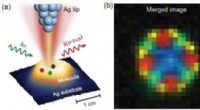
- Raman-picoscopie scannen:een nieuwe methode voor het bepalen van de moleculaire chemische structuur
- Nieuwe microfluïdische chip verhoogt de gevoeligheid van immunoassays met 1000x

- Simulaties verklaren detonatie-eigenschappen in TATB

 Het decoderen van een mRNA -bericht in een eiwit staat bekend als wat?
Het decoderen van een mRNA -bericht in een eiwit staat bekend als wat?  Wat is de kleur en het type rots dat oceanische korst vormt bij mid -oceaan richels?
Wat is de kleur en het type rots dat oceanische korst vormt bij mid -oceaan richels?  IJskristallen veroorzaken prachtige nachtlichtende wolken
IJskristallen veroorzaken prachtige nachtlichtende wolken  Fermilab-wetenschappers leiden zoektocht naar ongrijpbare vierde soort neutrino
Fermilab-wetenschappers leiden zoektocht naar ongrijpbare vierde soort neutrino Efficiënte nabij-infrarode luminescentie in met lanthanide gedoteerde, volledig anorganische halide dubbele perovskieten
Efficiënte nabij-infrarode luminescentie in met lanthanide gedoteerde, volledig anorganische halide dubbele perovskieten Klinkende raketlanceringen om aurora's te bestuderen
Klinkende raketlanceringen om aurora's te bestuderen Wat is een stof zonder water?
Wat is een stof zonder water?  Hoe de totale oppervlakte
Hoe de totale oppervlakte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

