
Wetenschap
Beschrijven als een reeks stappen Wat gebeurt er met suikermoleculen wanneer ze oploven in water?
Stap 1:Hydratatie
* Watermoleculen omringen de suikermoleculen. Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde hebben (waterstof) en een enigszins negatief uiteinde (zuurstof). Suikermoleculen zijn ook polair, waarbij hun hydroxylgroepen (OH) een vergelijkbare positieve en negatieve ladingsverdeling creëren.
* De positieve uiteinden van watermoleculen trekken de negatieve uiteinden van de suikermoleculen aan, en vice versa. Deze aantrekkingskracht, een "waterstofbinding" genoemd, vormt zich tussen de watermoleculen en de suikermoleculen.
Stap 2:Verstoring van de suikerkristalstructuur
* De sterke hydratatiekrachten overwinnen de zwakke krachten die de suikermoleculen in het kristalrooster houden. Dit breekt het suikerkristal uit elkaar in afzonderlijke suikermoleculen.
Stap 3:Dispersie
* De suikermoleculen worden omringd door watermoleculen en worden door de oplossing verspreid. Ze vormen niet langer een vaste structuur, maar bestaan eerder als individuele moleculen omgeven door water.
Stap 4:Equilibrium
* Het oplossende proces gaat door totdat een evenwichtspunt is bereikt. Dit betekent dat de snelheid waarmee suikermoleculen oplossen gelijk is aan de snelheid waarmee ze opnieuw kristalliseren. De oplossing is nu verzadigd, wat betekent dat het geen opgeloste suiker kan vasthouden.
Belangrijke punten om te onthouden:
* oplossen betekent niet dat de suikermoleculen verdwijnen. Ze veranderen gewoon van een vaste kristallijne structuur naar individuele moleculen omgeven door water.
* Suiker lost op vanwege de aantrekkingskracht tussen watermoleculen en suikermoleculen. Dit komt door hun polaire aard en de vorming van waterstofbruggen.
* Het proces is omkeerbaar. Als het water verdampt, zullen de suikermoleculen opnieuw kristalliseren.
 Aboriginal-groep dringt aan op reset van mijnbouw nadat oude site is vernietigd
Aboriginal-groep dringt aan op reset van mijnbouw nadat oude site is vernietigd Honderdduizenden vluchten Amerikaanse kust voor orkaan Laura
Honderdduizenden vluchten Amerikaanse kust voor orkaan Laura Aarde wetenschap omvat welke andere takken van wetenschap?
Aarde wetenschap omvat welke andere takken van wetenschap?  Hoe vormden de natuurlijke hulpbronnen levens van inheemse mensen in het zuidwesten?
Hoe vormden de natuurlijke hulpbronnen levens van inheemse mensen in het zuidwesten?  Wat als de VS stoppen met klimaatdeal? Ziet er niet goed uit voor de aarde
Wat als de VS stoppen met klimaatdeal? Ziet er niet goed uit voor de aarde
Hoofdlijnen
- Welke organel functioneert als de plaats van eiwitsynthese in cel?
- Hoe stamcellen worden gereguleerd
- Het proces waarmee een stationaire cel kleine deeltjes inneemt?
- Onderzoekers verkrijgen een momentopname die verduidelijkt hoe materialen cellen binnendringen
- Welke twee classificatiegroepen worden in een wetenschappelijke naam gebruikt?
- Hoe een verandering van één gen leidde tot nieuwe soorten Monkeyflower
- Wat is de gebruikelijke reactie in de populatiegrootte van veel soorten?
- Worden wetenschappelijke ontdekkingen aangestuurd door geweldige individuen of teams?
- Welk bloedgroep brengt zuurstof dicht bij cellen?
- Met suiker bedekte wereld

- Innovatieve combinatie van harde en zachte materialen verbetert de hechting op ruwe oppervlakken

- Sous-vide kookmethode maakt rundvleeseiwit beter verteerbaar

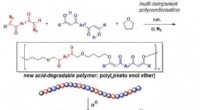
- Nieuw synthetisch polymeer afbreekbaar onder zeer milde zure omstandigheden
- Ontwerpen van het perfecte membraan voor schone scheiding van gassen

 Als de massa wordt verdubbeld, zal kinetische energie.?
Als de massa wordt verdubbeld, zal kinetische energie.?  Welke Arer Carnivor?
Welke Arer Carnivor?  Hoe kan koolstofdioxide worden verzameld?
Hoe kan koolstofdioxide worden verzameld?  Wat zijn de carrières met betrekking tot geologie en fotografie?
Wat zijn de carrières met betrekking tot geologie en fotografie?  Wat is 1 revolutie gelijk in hoeksnelheid?
Wat is 1 revolutie gelijk in hoeksnelheid?  Verspilde vogelveren veranderd in voedsel
Verspilde vogelveren veranderd in voedsel Is Sun een hoofdreeksster?
Is Sun een hoofdreeksster?  Hoe kan een object met een constante snelheid niet -nul versnelling hebben?
Hoe kan een object met een constante snelheid niet -nul versnelling hebben?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

