
Wetenschap
Welke deeltjes werken samen om atomen zich als vaste stoffen te laten gedragen?
* atomen: De bouwstenen van alle materie. Ze bestaan uit protonen, neutronen en elektronen.
* elektronen: Deze deeltjes zijn verantwoordelijk voor de chemische bindingen die atomen bij elkaar houden in een vaste stof. Er zijn twee hoofdtypen obligaties:
* ionische bindingen: Tijdens het ene atoom doneert een elektron aan het andere en vormt geladen ionen die elkaar sterk aantrekken.
* Covalente bindingen: Tijdens twee atomen delen elektronen, wat resulteert in een sterke aantrekkingskracht daartussen.
* intermoleculaire krachten: Zelfs wanneer atomen bij elkaar worden gehouden door sterke bindingen, zijn er zwakkere krachten die moleculen aantrekken aan elkaar. Deze krachten zijn cruciaal voor het bepalen van de eigenschappen van vaste stoffen:
* van der Waals krachten: Deze zwakke attracties ontstaan door tijdelijke schommelingen in elektronenverdeling rond moleculen.
* Waterstofbindingen: Deze zijn sterker dan van der Waals -krachten en treden op wanneer waterstofatomen worden gebonden aan sterk elektronegatieve atomen zoals zuurstof of stikstof.
Hoe deze interacties vaste eigenschappen creëren:
* Vaste vorm en volume: Vanwege de sterke bindingen en intermoleculaire krachten worden atomen gehouden in een vaste, rigide structuur. Dit geeft vaste stoffen hun karakteristieke vorm en volume.
* Hoge dichtheid: De nauwe verpakking van atomen in vaste stoffen resulteert in een hoge dichtheid in vergelijking met vloeistoffen of gassen.
* Weerstand tegen compressie: Sterke bindingen en krachten maken vaste stoffen moeilijk te comprimeren.
* stijfheid en elasticiteit: Vaste stoffen kunnen vervorming onder stress weerstaan vanwege de sterke bindingen die ze bij elkaar houden.
Samenvattend: Het is de combinatie van sterke chemische bindingen die atomen aan elkaar houden en zwakkere intermoleculaire krachten die moleculen bij elkaar houden die het gedrag van een vaste stof definiëren.
 Hoe verschilt de tijdtemperatuurkoelcurve van een eutectische samenstelling van een legering van dat een puur metaal?
Hoe verschilt de tijdtemperatuurkoelcurve van een eutectische samenstelling van een legering van dat een puur metaal?  Waarom is kopersulfaatblauw in water?
Waarom is kopersulfaatblauw in water?  Hoeveel valentie-elektronen heeft cl-?
Hoeveel valentie-elektronen heeft cl-?  Hoe schrijf je een vergelijking voor de reactie van butylamine met HCl?
Hoe schrijf je een vergelijking voor de reactie van butylamine met HCl?  Hoe beïnvloeden elektronen de vorm van een molecuul?
Hoe beïnvloeden elektronen de vorm van een molecuul?
 Wat voor soort vogels eten bijen?
Wat voor soort vogels eten bijen?  Wat verwijst naar de warmte of kou van een object?
Wat verwijst naar de warmte of kou van een object?  Heatstruck Italië begint zijn dorstige wijnstokken te oogsten
Heatstruck Italië begint zijn dorstige wijnstokken te oogsten Yellowstone verliest zijn sneeuw naarmate het klimaat warmer wordt, wijdverbreide problemen voorspellen voor water en dieren in het wild
Yellowstone verliest zijn sneeuw naarmate het klimaat warmer wordt, wijdverbreide problemen voorspellen voor water en dieren in het wild Soorten scrubbers
Soorten scrubbers
Hoofdlijnen
- Wat is de rol van agar -ingrediënt in kweekmedium?
- Wat omvat de procestekst in de wetenschap?
- Mensen zijn samengesteld uit welke cellen?
- Welk systeem is verantwoordelijk voor het verzamelen en reageren op informatie?
- Wat is de definitie van pyrogenen?
- Waarom de harde Sneeuwbalaarde onze vroegste meercellige voorouders op gang bracht
- Hoe worden enzym meestal genoemd?
- Wat is de locatie van DNA in een prokaryotische cel?
- Vogels versus bijen:studie helpt verklaren hoe bloemen evolueerden om bestuivers te specialiseren
- Bacterieval kan antibioticaresistentie helpen vertragen
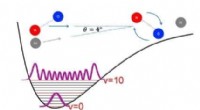
- De studie van niet-covalente intermoleculaire interacties naar een nieuw gebied duwen
- Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden

- Het beroemde Zelinsky-proces onthuld:zelfbevorderende acetylenische cascade produceert benzeen

- Licht schijnend op recombinatiemechanismen in zonnecelmaterialen
 Standaardiseren HCL met behulp van NA2CO3 -titratie. Textbook zegt dat de oplossing op het equivalentiepunt enigszins zuur is. het en waarom?
Standaardiseren HCL met behulp van NA2CO3 -titratie. Textbook zegt dat de oplossing op het equivalentiepunt enigszins zuur is. het en waarom?  Welke fase van de celcyclus zijn typecellen in uw lichaam die niet langer mitoses ondergaan?
Welke fase van de celcyclus zijn typecellen in uw lichaam die niet langer mitoses ondergaan?  Welk type energie kan niet worden gemaakt of vernietigd?
Welk type energie kan niet worden gemaakt of vernietigd?  Welke industrieën gebruiken microscopen?
Welke industrieën gebruiken microscopen?  Wat is een overlevingsgen in evolutie?
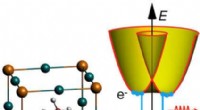
Wat is een overlevingsgen in evolutie?  Vooruitgang in topologische faseovergang in organometaalroosters
Vooruitgang in topologische faseovergang in organometaalroosters  Kan een deeltje in één dimensionaal met nulsnelheid niet -snelheid hebben?
Kan een deeltje in één dimensionaal met nulsnelheid niet -snelheid hebben?  Wanneer was Peninsulares?
Wanneer was Peninsulares?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

