
Wetenschap
Waarom vormen atomen van niet -metalen anionen terwijl metalen kationen?
1. Elektronenconfiguratie:
* metalen: Metalen hebben over het algemeen een paar elektronen in hun buitenste schaal (valentieschaal). Ze hebben de neiging om deze elektronen te verliezen om een stabiele elektronenconfiguratie te bereiken, die vaak lijkt op het dichtstbijzijnde edelgas. Het verliezen van elektronen creëert een positieve lading , resulterend in een kation.
* niet -metalen: Niet -metalen hebben veel elektronen in hun buitenste schaal, vaak dicht bij een volledige schaal. Ze hebben de neiging om elektronen te krijgen om hun buitenste schaal te voltooien en een stabiele elektronenconfiguratie te bereiken zoals een edelgas. Elektronen verkrijgen creëert een negatieve lading , resulterend in een anion.
2. Elektronegativiteit:
* metalen: Metalen hebben meestal een lage elektronegativiteit, wat betekent dat ze een zwakkere aantrekkingskracht hebben op elektronen. Hierdoor worden ze meer kans om elektronen te verliezen en kationen te worden.
* niet -metalen: Niet -metalen hebben een hoge elektronegativiteit, hetgeen een sterke aantrekkingskracht voor elektronen aangeeft. Hierdoor worden ze meer kans om elektronen te krijgen en anionen te worden.
3. Ionisatie -energie:
* metalen: Metalen hebben relatief lage ionisatie -energieën, wat betekent dat er minder energie voor nodig is om een elektron te verwijderen. Hierdoor worden ze meer kans om elektronen te verliezen en kationen te worden.
* niet -metalen: Niet -metalen hebben hoge ionisatie -energieën, die meer energie vereisen om een elektron te verwijderen. Hierdoor verliezen ze minder kans om elektronen te verliezen en meer kans om elektronen te krijgen en anionen te worden.
Voorbeeld:
* natrium (NA): Natrium is een metaal met één valentie -elektron. Het verliest gemakkelijk dit elektron om een Na+ -kation te worden, waardoor de stabiele elektronenconfiguratie van Neon (NE) wordt bereikt.
* chloor (CL): Chloor is een niet -metaal met zeven valentie -elektronen. Het krijgt gemakkelijk één elektron om een cl-anion te worden, waardoor de stabiele elektronenconfiguratie van argon (AR) wordt bereikt.
Samenvattend:
De neiging van metalen om elektronen en niet -metalen te verliezen om elektronen te winnen wordt aangedreven door hun wens om een stabiele elektronenconfiguratie te bereiken. Dit verschil in elektronengedrag wordt weerspiegeld in hun elektronegativiteit, ionisatie -energie en leidt uiteindelijk tot de vorming van kationen voor metalen en anionen voor niet -metalen.
 Hoeveel mol broomgas staat er in 37,7 gram?
Hoeveel mol broomgas staat er in 37,7 gram?  Waarom zeggen sommige mensen dat waterstof boven Lithium Li en anderen moet zijn, beweren dat het fluor F?
Waarom zeggen sommige mensen dat waterstof boven Lithium Li en anderen moet zijn, beweren dat het fluor F?  Hoe zijn atomen gerelateerd aan moleculen in een monster van verbinding?
Hoe zijn atomen gerelateerd aan moleculen in een monster van verbinding?  Is SO2 een metaal of niet -metaal?
Is SO2 een metaal of niet -metaal?  Waarom is constante temperatuur belangrijk in een experiment?
Waarom is constante temperatuur belangrijk in een experiment?
 NASA-NOAA's Suomi NPP volgt vuur en rook van twee continenten
NASA-NOAA's Suomi NPP volgt vuur en rook van twee continenten Dag nul uitstellen:investering in waterefficiëntie houdt kranen draaiende
Dag nul uitstellen:investering in waterefficiëntie houdt kranen draaiende Heeft zwak licht 's nachts invloed op de gezondheid van motten en andere insecten?
Heeft zwak licht 's nachts invloed op de gezondheid van motten en andere insecten?  Oplosbaar ijzer in de lucht boven Chinese steden kan gezondheidsrisico's opleveren, studie vondsten
Oplosbaar ijzer in de lucht boven Chinese steden kan gezondheidsrisico's opleveren, studie vondsten Tsunamisignalen om afkalven van gletsjers in Groenland te meten
Tsunamisignalen om afkalven van gletsjers in Groenland te meten
Hoofdlijnen
- Hoe menselijke transportgewoonten het gedrag van kleine mijten helpen verklaren
- Genetisch onderzoek streeft een ongrijpbaar doel na:hoeveel bultruggen bestonden er vóór de walvisvangst?
- Hoe is een wetenschapper die de populatie bestudeert?
- Hoe wordt het woord gedefinieerd?
- Wetenschappers identificeren hoe de ontwikkeling van verschillende soorten dezelfde genen met verschillende kenmerken gebruikt
- Wat is selectieve permeabiliteit en waarom het belangrijk is voor cellen?
- Een hete start van het ontstaan van het leven? Onderzoekers brengen de eerste chemische bindingen in kaart die uiteindelijk DNA opleveren
- Wat is de betekenis van dermale ostia in zoölogie?
- Waarom stinkt de stinkplant?
- Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels

- Studie gebruikt neutronen om licht te laten schijnen op het afsluiten van kankercellen

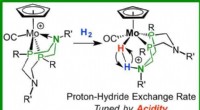
- Wetenschappers bepalen de snelheid van het breken en fixeren van diwaterstofmoleculen
- Dit draagbare apparaat camoufleert zijn drager, ongeacht het weer

- Wetenschappers vinden een verband tussen kanker en veroudering in onze cellen

 Standpunt:Figuren als Andrew Tate kunnen vrouwenhaat helpen verspreiden. Maar ze versterken het probleem, en veroorzaken het niet
Standpunt:Figuren als Andrew Tate kunnen vrouwenhaat helpen verspreiden. Maar ze versterken het probleem, en veroorzaken het niet  Er zijn aanwijzingen dat veel tornado's groter en sterker zijn dan gerapporteerd
Er zijn aanwijzingen dat veel tornado's groter en sterker zijn dan gerapporteerd Waarom klikt elektrische ventilator en licht wanneer de stroom wordt ingeschakeld?
Waarom klikt elektrische ventilator en licht wanneer de stroom wordt ingeschakeld?  Weet je moeder het?
Weet je moeder het?  Wat zijn de belangrijkste natuurlijke kenmerken van Malawi?
Wat zijn de belangrijkste natuurlijke kenmerken van Malawi?  Wat hebben sterke zuren gemeen met ionische verbindingen?
Wat hebben sterke zuren gemeen met ionische verbindingen?  Nieuwe theorie suggereert dat uraniumsneeuwvlokken in witte dwergen een stervernietigende explosie kunnen veroorzaken
Nieuwe theorie suggereert dat uraniumsneeuwvlokken in witte dwergen een stervernietigende explosie kunnen veroorzaken Van militair tot mainstream:de evolutie van de AR-15
Van militair tot mainstream:de evolutie van de AR-15
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

