
Wetenschap
Hoe ben je nucleaire bindende energie berekenen?
het berekenen van nucleaire bindingsenergie
Nucleaire bindingsenergie (BE) is de energie die nodig is om alle nucleonen (protonen en neutronen) in de kern van een atoom te scheiden. Hier is hoe u het kunt berekenen:
1. Bepaal het massafefect:
* massa -defect (ΔM): Dit is het verschil tussen de massa van de kern en de som van de massa's van zijn individuele protonen en neutronen.
* formule: ΔM =(zm p + Nm n ) - M nucleus
* Z =Atomisch nummer (aantal protonen)
* N =neutronennummer (aantal neutronen)
* M p =Massa van een proton (1,00727647 AMU)
* m n =Massa van een neutron (1,00866492 AMU)
* M Nucleus =Massa van de kern (experimenteel gemeten)
2. Converteer het massafefect naar energie:
* Einstein's beroemde vergelijking: E =ΔMc
2
* E =bindende energie
* ΔM =massa -defect (in atomaire massa -eenheden - amu)
* C =Lichtsnelheid (2.99792458 x 10
8
mevrouw)
3. Druk de energie uit in de gewenste eenheid:
* Gemeenschappelijke eenheden:
* mev (megaelectron volt): 1 AMU =931.494 MeV
* Joules: 1 AMU =1.49242 x 10
-10
J
Voorbeeld:
Laten we de bindende energie van helium-4 berekenen (
1. Massafefect:
* Z =2 (aantal protonen)
* N =2 (aantal neutronen)
* M p =1,00727647 AMU
* m n =1,00866492 Amu
* M Nucleus =4,00260325 AMU (experimentele waarde)
* Δm =(2 * 1.00727647 + 2 * 1.00866492) - 4.00260325 =0.030378 Amu
2. Energieconversie:
* E =0.030378 AMU * 931.494 MEV/AMU =28.295 MEV
Daarom is de bindende energie van helium-4 28.295 MeV.
Opmerking:
* Bindende energie is een positieve waarde, die de energie vertegenwoordigt die vrijkomt wanneer de nucleonen samen in de kern zijn gebonden.
* Hoe hoger de bindende energie per nucleon, hoe stabieler de kern.
* Deze berekening geeft de totale bindende energie. U kunt ook de bindende energie per nucleon berekenen door de totale bindende energie te delen door het aantal nucleonen.
Deze methode geeft een goede benadering van de bindende energie, maar het is belangrijk om te onthouden dat experimentele waarden enigszins kunnen verschillen.
 Stress en inspanning:geochemici beantwoorden fundamentele vraag over minerale reacties
Stress en inspanning:geochemici beantwoorden fundamentele vraag over minerale reacties Studie onderzoekt hoe DNA-schade wordt gerepareerd door antioxiderende enzymen
Studie onderzoekt hoe DNA-schade wordt gerepareerd door antioxiderende enzymen  Neutronen bieden de eerste blik op een levend celmembraan op nanoschaal
Neutronen bieden de eerste blik op een levend celmembraan op nanoschaal Welk membraan vindt lichte reacties plaats?
Welk membraan vindt lichte reacties plaats?  Hoeveel protonen heeft één atoom van element natrium?
Hoeveel protonen heeft één atoom van element natrium?
Hoofdlijnen
- Waarom wisten vroege Grieken niet veel over het menselijk lichaam?
- Hoe handelen planten snel om infecties te bestrijden?
- Ontdekking van aminozuur onthult hoe licht huidmondjes in planten open maakt
- Waarom vormen de fosfolipiden Sourround -cel een dubbellaag?
- Wat is de wetenschappelijke gemeenschappelijke naam voor gastro -intestinale ziekte?
- Het symposium in Pittsburgh antwoordt:Wat is Watson?
- Zijn er slechts 3 soorten wetenschap?
- Wie zijn ontdekte structuur van DNA?
- Wat is een beschreven cel met paren chromosomen?
- Synthese bij hoge temperatuur onder druk helpt eigenschappen van metalen en keramiek te combineren

- Onderzoekers ontwikkelen nanoporeuze super-multi-elementenkatalysator

- Hydrogel bevordert wondgenezing beter dan traditionele zwachtels, gaasjes
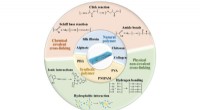
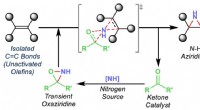
- Wetenschappers vereenvoudigen toegang tot bouwstenen voor medicijnen
- Wetenschappers produceren eerste open source all-atom-modellen van COVID-19 spike-eiwit

 Guinness World Records noemt grafeen-aerogel als 's werelds minst dichte 3D-geprinte structuur
Guinness World Records noemt grafeen-aerogel als 's werelds minst dichte 3D-geprinte structuur Demystificatie van de complexe aard van arctische wolken
Demystificatie van de complexe aard van arctische wolken  Het gezondheidseffect van luchtvervuiling door het verkeer
Het gezondheidseffect van luchtvervuiling door het verkeer Topologische isolatoren verbinden met magnetische materialen voor energiezuinige elektronica
Topologische isolatoren verbinden met magnetische materialen voor energiezuinige elektronica Prototype elektrisch vliegtuig neemt eerste vlucht
Prototype elektrisch vliegtuig neemt eerste vlucht Hoe is het begrip van elektriciteit in de loop van de tijd veranderd?
Hoe is het begrip van elektriciteit in de loop van de tijd veranderd?  Studie bekijkt hoe landaankopen de klimaatverandering beïnvloeden
Studie bekijkt hoe landaankopen de klimaatverandering beïnvloeden Hoe kleine watermonsters echt grote dieren kunnen vinden
Hoe kleine watermonsters echt grote dieren kunnen vinden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

