
Wetenschap
Welke fasen gaat een vaste stof door bij het verhit?
1. vaste fase: De vaste stof bevindt zich in zijn aanvankelijke, rigide toestand. De deeltjes zijn nauw gepakt en trillen in vaste posities.
2. smelten: Naarmate warmte wordt toegevoegd, trillen de deeltjes sneller en breken ze los van hun vaste posities. Dit is het smeltpunt , waar de vaste overgangen naar een vloeistof.
3. vloeibare fase: De deeltjes bewegen nu vrij en kunnen langs elkaar glijden.
4. koken: Naarmate meer warmte wordt toegevoegd, krijgen de deeltjes voldoende energie om de aantrekkelijke krachten te overwinnen die ze in de vloeibare toestand houden. Dit is het kookpunt , waar de vloeistof overgaat in een gas.
5. gasfase: De deeltjes zijn nu wijd verdeeld en bewegen vrij en onafhankelijk.
Belangrijke opmerking: Dit is een vereenvoudigde verklaring. De werkelijke overgangen kunnen complexer zijn, afhankelijk van het type vaste stof en de betrokken druk. Sommige vaste stoffen kunnen bijvoorbeeld rechtstreeks van een vaste stof naar een gas sublimeren zonder een vloeibare fase te doorlopen.
 NASA vindt nieuwe tropische storm Iselle die al vecht tegen windschering
NASA vindt nieuwe tropische storm Iselle die al vecht tegen windschering Echokamers volharden in klimaatpolitiek, uit onderzoek blijkt
Echokamers volharden in klimaatpolitiek, uit onderzoek blijkt Onderwater ijsterras waargenomen aan de voorkant van Grey Glacier
Onderwater ijsterras waargenomen aan de voorkant van Grey Glacier Desert Ecosystems for Kids
Desert Ecosystems for Kids NASA ziet overblijfselen van ex-tropische cycloon Beryls vechten om te overleven
NASA ziet overblijfselen van ex-tropische cycloon Beryls vechten om te overleven
Hoofdlijnen
- Science Fair-projecten met nagellak
- Indringende vraag:Wat gaat er verloren als een taal sterft?
- Waarom vereist chemiososmose een membraan?
- Inzicht in hoe cellen reageren op fysieke signalen zou tot nieuwe ziektebehandelingen kunnen leiden
- Welke verhouding in eukaryotische cellen coderen voor eiwitten of structureel RNA?
- Helpen kunstmatige slaapplaatsen vleermuizen? Experts zeggen dat er meer onderzoek nodig is
- Welke vormen over het midden van een cel nabij het einde van Telophase?
- Grote meercellige mariene algen worden genoemd?
- Natuurlijke selectie veroorzaakt veranderingen in populaties van organismen die niet individueel zijn omdat?
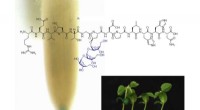
- Gemodificeerde peptiden kunnen de groei en ontwikkeling van planten stimuleren
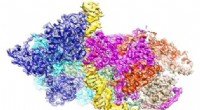
- Hi-res afbeelding van structuur van het oorsprongherkenningscomplex gebonden aan DNA onthuld
- Productie van waterstofperoxide opruimen

- schoner, sterker, harder:Nieuwe technologie verbetert duurzaam beton

- Verpakkingsmaterialen recyclebaar maken

 Waarom wordt kmno4 toegevoegd in eenvoudige destillatie?
Waarom wordt kmno4 toegevoegd in eenvoudige destillatie?  Heeft NH3 een polaire binding?
Heeft NH3 een polaire binding?  Een nieuwe katalysator voor efficiënte oxidatie van inactieve alkanen
Een nieuwe katalysator voor efficiënte oxidatie van inactieve alkanen  Groeiende Europese nanodraden
Groeiende Europese nanodraden Chloor- en kaliumjodide -evenwichtige vergelijking?
Chloor- en kaliumjodide -evenwichtige vergelijking?  Waarom hebben kleine sterren een langere levensduur dan grote sterren?
Waarom hebben kleine sterren een langere levensduur dan grote sterren?  Is indium belangrijk voor levende wezens?
Is indium belangrijk voor levende wezens?  Wat is de kracht die tegen drijfvermogen handelt?
Wat is de kracht die tegen drijfvermogen handelt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

