
Wetenschap
Waarom zijn atomaire nummers radioactief?
* Atomisch nummer Verwijst naar het aantal protonen in de kern van een atoom. Het definieert het element waartoe het atoom behoort. Alle koolstofatomen hebben bijvoorbeeld een atoomnummer van 6 omdat ze 6 protonen hebben.
* radioactiviteit verwijst naar de spontane emissie van deeltjes of energie uit de kern van een atoom. Dit gebeurt omdat sommige isotopen (atomen van hetzelfde element met verschillende aantallen neutronen) onstabiele kernen hebben die vervallen om stabieler te worden.
Dit is waarom de verklaring verkeerd is:
1. Atomisch nummer zelf is niet radioactief. Het atoomnummer vertelt u alleen het aantal protonen, niet het aantal neutronen. Het is de * combinatie * van protonen en neutronen in de kern die bepaalt of een atoom radioactief is of niet.
2. Radioactieve isotopen bestaan voor veel elementen met verschillende atoomnummers. Bijvoorbeeld, koolstof-14 (radioactief) en koolstof-12 (stabiel) hebben beide een atoomnummer van 6.
3. Niet alle atomen met hoge atoomnummers zijn radioactief. Hoewel elementen met hoge atoomnummers de neiging hebben om meer onstabiele isotopen te hebben, hebben sommige ook stabiele isotopen.
samenvatten:
* Atomische getallen definiëren elementen.
* Radioactiviteit is een eigenschap van onstabiele isotopen, niet het atoomnummer zelf.
Het is belangrijk om onderscheid te maken tussen deze concepten om de aard van atomen te begrijpen en hoe ze zich gedragen.
 De koffiecrème en suiker zullen gemakkelijk oplossen in koud water waarom of niet?
De koffiecrème en suiker zullen gemakkelijk oplossen in koud water waarom of niet?  Wat is de vergelijking voor natriumfosfaat en water?
Wat is de vergelijking voor natriumfosfaat en water?  Zijn oxiden van niet-metalen zuur of basisch en waarom?
Zijn oxiden van niet-metalen zuur of basisch en waarom?  Welke intermoleculaire krachten beschrijven het beste waarom moleculen zoals CF3CF3 oplosbaar zijn in vloeibare CO2?
Welke intermoleculaire krachten beschrijven het beste waarom moleculen zoals CF3CF3 oplosbaar zijn in vloeibare CO2?  Waarom won Frederick Sanger de Nobelprijs in de chemie 1958?
Waarom won Frederick Sanger de Nobelprijs in de chemie 1958?
 Geavanceerde biobrandstoffen zijn veelbelovend voor de vervanging van sommige fossiele brandstoffen
Geavanceerde biobrandstoffen zijn veelbelovend voor de vervanging van sommige fossiele brandstoffen Waarom gebruik je modellen om de natuur te beschrijven?
Waarom gebruik je modellen om de natuur te beschrijven?  Nieuwe bevindingen werpen licht op de grote milieuverschuiving door het Midden-Eoceen in Zuid-China
Nieuwe bevindingen werpen licht op de grote milieuverschuiving door het Midden-Eoceen in Zuid-China Eén graad opwarming van de aarde veroorzaakt een 50% toename van het risico op ontheemding
Eén graad opwarming van de aarde veroorzaakt een 50% toename van het risico op ontheemding Zwerfvuilprobleem aan de beschermde kusten van Engeland
Zwerfvuilprobleem aan de beschermde kusten van Engeland
Hoofdlijnen
- Hoe kun je zien of een cel chlorofyl bevat?
- Wat is vervangende klonen?
- Vissers in Istanbul houden traditie in stand ondanks voorraadalarm
- Wat zijn menselijke eters?
- Haaien vertonen nieuwe veranderingen in hun immuunkankergerelateerde genen
- Hoe relateer je de niveaus van orgaansystemen aan elkaar en het hele systeem of organisme?
- Hoe noem je een persoon die zwaartekracht en vaccins bestudeert?
- Wat is het belangrijkste aspect van de biologie van het dagelijkse leven?
- Wat is Supplex Nylon?
- Nieuwe flexibele en taaie superelastische metaallegering is veelbelovend in biomedische toepassingen

- Nieuw gesynthetiseerde schimmelverbinding kan een zelfvernietigingsknop voor kanker inschakelen
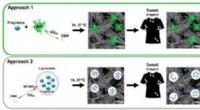
- Geurafgevende stof kan zweterige gymkleding helpen neutraliseren
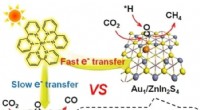
- Enkele goudatomen katalyseren de selectieve methanisering van kooldioxide
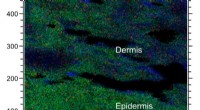
- Nieuwe methode brengt chemicaliën in de huid in kaart
 In welk type klimaat worden naaldbos gevonden?
In welk type klimaat worden naaldbos gevonden?  Wat is het nut van zomertijd?
Wat is het nut van zomertijd?  De dikke bol van kometen die het zonnestelsel omcirkelen tot een afstand die ongeveer 50000 AU wordt genoemd?
De dikke bol van kometen die het zonnestelsel omcirkelen tot een afstand die ongeveer 50000 AU wordt genoemd?  Onderzoekers meten de mechanica van kankercellen bij levende dieren met behulp van nanodeeltjes
Onderzoekers meten de mechanica van kankercellen bij levende dieren met behulp van nanodeeltjes Afbeelding:Hubble ziet vaag sterrenstelsel
Afbeelding:Hubble ziet vaag sterrenstelsel Seymour Benzer
Seymour Benzer  Wat zijn de namen van hoofdsterren?
Wat zijn de namen van hoofdsterren?  Wat maakt iets een theorie in de wetenschap?
Wat maakt iets een theorie in de wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

