
Wetenschap
Hoe atoom is onstabiel?
1. Radioactief verval:
* onstabiele kernen: Sommige atomen hebben een onstabiele kern, wat betekent dat de balans tussen protonen en neutronen is uitgeschakeld.
* Radioactieve isotopen: Deze isotopen hebben overtollige energie, die ze vrijgeven in de vorm van straling. Deze straling kan alfa -deeltjes, bèta -deeltjes of gammastralen zijn.
* Soorten verval: Verschillende vervalprocessen treden op om de kern te stabiliseren, zoals alfa -verval (een alfa -deeltje uitzenden), bèta -verval (een elektron of positron uitzenden) of gamma -verval (een gamma -straal uitzenden).
* halfwaardetijd: Radioactief verval gebeurt met een specifiek tempo, gemeten door een halfwaardetijd, wat de tijd is die nodig is voor de helft van de radioactieve atomen in een monster om te vervallen.
2. Opgewonden toestand:
* elektronen: Elektronen in atomen kunnen worden geëxciteerd naar hogere energieniveaus door energie te absorberen (bijvoorbeeld van licht).
* Terug naar grondtoestand: Deze geëxciteerde elektronen keren de neiging terug te keren naar hun lagere energietoestanden, waardoor de overtollige energie als licht of warmte wordt vrijgegeven.
3. Ionisatie:
* winst of verlies van elektronen: Atomen kunnen elektronen winnen of verliezen om ionen te worden, die geladen deeltjes zijn. Deze ladingsverandering kan het atoom onstabiel maken, omdat het niet langer een neutrale lading heeft.
4. Chemische reacties:
* bindingen: Atomen kunnen chemische bindingen vormen met andere atomen om een stabielere toestand te bereiken. Dit omvat vaak het delen of overbrengen van elektronen om hun buitenste elektronenschalen te vullen.
* Reactiviteit: Hoe onstabieler een atoom is, hoe groter de kans dat het is om deel te nemen aan chemische reacties om stabiliteit te bereiken.
Voorbeeld:
* carbon-14: Carbon-14 is een radioactieve isotoop van koolstof met een halfwaardetijd van 5.730 jaar. Het vervalt door bèta-verval, uitstraalt een elektron en wordt stikstof-14.
Sleutelpunten:
* Atomen streven naar stabiliteit, wat vaak wordt bereikt door een gebalanceerde kern en een volledige buitenste elektronenschil te hebben.
* Onstabiele atomen ondergaan processen zoals radioactief verval, excitatie of ionisatie om stabiliteit te bereiken.
* Deze processen geven vaak energie af in de vorm van straling, licht of warmte.
 Extreme hittegolven in Zuid- en Zuidoost-Azië zijn een teken van wat komen gaat
Extreme hittegolven in Zuid- en Zuidoost-Azië zijn een teken van wat komen gaat  Onderzoekers bieden een unieke manier om de koolstofemissies in waterlichamen te monitoren
Onderzoekers bieden een unieke manier om de koolstofemissies in waterlichamen te monitoren  Hoe zit het met de recente wilde tornado's? Deskundige weegt mee
Hoe zit het met de recente wilde tornado's? Deskundige weegt mee  Hoe het weer kan worden beschreven voor Preschoolers
Hoe het weer kan worden beschreven voor Preschoolers Onder druk:hoe kamgelei zich heeft aangepast aan het leven op de bodem van de oceaan
Onder druk:hoe kamgelei zich heeft aangepast aan het leven op de bodem van de oceaan
Hoofdlijnen
- Nieuwsgierige grote witte haai speelt met camera
- Stadia van ecologische successie
- Wat is een Hullocigen?
- Is rijst een vasculaire of niet -vasculaire plant?
- Hoe Body Dysmorphic Disorder werkt
- Waar betekent gespecialiseerde cellen?
- Hoe de vlieg zijn reproductieve mannetje selecteert
- Waarom zijn wij wetenschap?
- Het verschil tussen orthologe en paralogische genen
- Programmeer pH:nieuwe techniek kan DNA-synthese versnellen

- Microstaafjes gemaakt van lanthanoïde organische raamwerken fungeren als optische golfgeleiders op microschaal

- Nieuwe methode belooft minder bijwerkingen van kankermedicijnen

- Hoe een bepaald eiwit tot tweederde van de methaanemissie ter wereld regelt
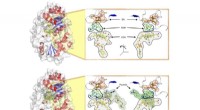
- Weg geopend om afval bij het opvangen van zonne-energie te minimaliseren
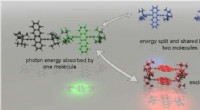
 Miniatuurdruppels kunnen een raadsel over de oorsprong van het leven oplossen
Miniatuurdruppels kunnen een raadsel over de oorsprong van het leven oplossen Intermoleculaire krachten in de structuur van propaan
Intermoleculaire krachten in de structuur van propaan Hoe wordt snelheid gemeten in vliegtuigen?
Hoe wordt snelheid gemeten in vliegtuigen?  Toekomst van mobiliteit:enkele wilde ritten vooruit op tech show
Toekomst van mobiliteit:enkele wilde ritten vooruit op tech show Wat is het proces waarmee bloedmanen worden veroorzaakt en welke factoren bijdragen aan hun unieke uiterlijk in de nachtelijke hemel?
Wat is het proces waarmee bloedmanen worden veroorzaakt en welke factoren bijdragen aan hun unieke uiterlijk in de nachtelijke hemel?  Welk apparaat wordt gebruikt om elektriciteit van zonne -energie om te zetten?
Welk apparaat wordt gebruikt om elektriciteit van zonne -energie om te zetten?  US Navy kijkt naar grafeen nanoribbon voor ultiem energiecontrolesysteem
US Navy kijkt naar grafeen nanoribbon voor ultiem energiecontrolesysteem Wat is de evenwichtige reactie wanneer lood II nitraat gemengd met calciumchloride?
Wat is de evenwichtige reactie wanneer lood II nitraat gemengd met calciumchloride?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

