
Wetenschap
Waarom lost een opgeloste stof sneller op in heet water?
1. Verhoogde kinetische energie:
- Hotwatermoleculen hebben hogere kinetische energie, wat betekent dat ze sneller bewegen en vaker botsen met de opgeloste deeltjes.
- Deze botsingen bieden de energie die nodig is om de bindingen te verbreken die de opgeloste deeltjes bij elkaar houden, waardoor ze zich kunnen verspreiden naar het oplosmiddel.
2. Verminderde viscositeit:
- Heet water is minder viskeus dan koud water, wat betekent dat het minder weerstand heeft tegen stroming.
- Dit zorgt voor een gemakkelijkere beweging van opgeloste deeltjes door het oplosmiddel, waardoor snellere oplossing wordt vergemakkelijkt.
3. Verhoogde oplosmiddelcapaciteit:
- Heet water kan meer opgeloste opgeloste stof bevatten dan koud water. Dit komt omdat de verhoogde kinetische energie van de watermoleculen hen in staat stelt om effectiever te interageren met de opgeloste moleculen, waardoor aantrekkelijke krachten tussen opgeloste stofdeeltjes worden overwinnen.
4. Verbeterde diffusie:
- De verhoogde kinetische energie van zowel oplosmiddel- als opgeloste deeltjes in heet water leidt tot snellere diffusie.
- Diffusie is het proces waardoor opgeloste moleculen zich over het oplosmiddel verspreiden, en snellere diffusie betekent dat de opgeloste stof sneller oplost.
5. Breek van waterstofbruggen:
- Voor sommige opgeloste stoffen, met name die welke waterstofbindingen vormen met water (bijv. Suikers), kan warmte deze bindingen verzwakken, waardoor het voor de opgeloste moleculen gemakkelijker wordt om te communiceren met het oplosmiddel.
Samenvattend: De verhoogde kinetische energie, verminderde viscositeit en verbeterde diffusie in heet water, gecombineerd met het verhoogde oplosmiddelcapaciteit en potentiële verzwakking van waterstofbruggen, dragen allemaal bij aan een snellere oplossing van een opgeloste stof.
Hoofdlijnen
- Wat zijn enkele wiggen in het menselijk lichaam?
- Hoe inheemse verbranding de bossen van de Klamath Mountains een millennium lang heeft gevormd
- Wat zijn de defecten van eenvoudige cel?
- De dichtheid van de Wolbachia-bacterie verandert per seizoen bij vlinders
- Waarom vormen bacteriën twee van het leven van de drie domeinen?
- Genotype & Phenotype Definitie
- H5N1-stam van vogelgriep gevonden in melk:WHO
- Wat vormt een nieuwe soort?
- Welk type nuclieczuur draagt de codes voor het maken van eiwitten van kern tot ribosoom?
- Kleine hoeveelheden virus detecteren bij vroege infecties
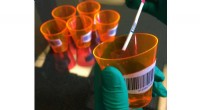
- Chemici kenmerken de dodelijke schimmel onder ons
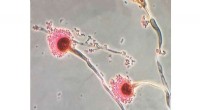
- Onderzoekers kijken met een frisse blik naar de Michaelis-Menten-vergelijking

- Methode om microfluïdische elektrochemische technologieën toe te passen op redox-neutrale reacties met één elektronoverdracht
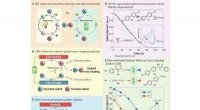
- Nieuwe strategie zorgt voor efficiënte en stabiele elektrolyse van kooldioxide in elektrolysecel voor vaste oxiden

 Wat is de lading van een atoom met één elektron meer dan protonen?
Wat is de lading van een atoom met één elektron meer dan protonen?  Heeft een vulkaan continentale of oceanische korst?
Heeft een vulkaan continentale of oceanische korst?  Welke planetendag duurt meer dan de helft van zijn jaar?
Welke planetendag duurt meer dan de helft van zijn jaar?  Nanoprobe maakt meting van eiwitdynamiek in levende cellen mogelijk
Nanoprobe maakt meting van eiwitdynamiek in levende cellen mogelijk Hé Siri:Hoeveel weegt dit cluster van sterrenstelsels?
Hé Siri:Hoeveel weegt dit cluster van sterrenstelsels?  Is de aarde tiende planeet van de zon?
Is de aarde tiende planeet van de zon?  Zijn er planeten van dezelfde grootte?
Zijn er planeten van dezelfde grootte?  Atomaire pingpong
Atomaire pingpong
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


