
Wetenschap
Waarom heeft pentane een hogere dichtheid dan 2-2-dimethylpropaan?
Dit is waarom:
* Vorm en verpakking: Pentane heeft een lineaire of enigszins vertakte structuur, wat betekent dat de moleculen steviger kunnen samenvoegen. Dit leidt tot een hogere dichtheid. 2,2-dimethylpropaan heeft daarentegen een zeer compacte, bolvormige vorm als gevolg van de vertakking aan de koolstofketen. Deze bolvormige vorm voorkomt efficiënte verpakking, wat resulteert in een lagere dichtheid.
* intermoleculaire krachten: Hoewel beide moleculen alleen de dispersiekrachten van Londen hebben (zwakke intermoleculaire krachten), zorgt de meer compacte structuur van 2,2-dimethylpropaan voor sterkere dispersiekrachten in Londen toe als gevolg van een groter oppervlak van interactie. Deze iets hogere intermoleculaire kracht draagt bij aan een hogere dichtheid.
Samenvattend:
* 2,2-dimethylpropaan (neopentaan) heeft een hogere dichtheid dan pentaan vanwege de compacte, sferische structuur, die een efficiëntere verpakking en sterkere intermoleculaire krachten mogelijk maakt.
Laat het me weten als je meer informatie wilt over dichtheid of intermoleculaire krachten!
 Waarom worden kleur gebruikt om mineralen te identificeren?
Waarom worden kleur gebruikt om mineralen te identificeren?  Zink of bron? Een nieuw model om organische koolstof in oppervlaktewater te meten
Zink of bron? Een nieuw model om organische koolstof in oppervlaktewater te meten  Wat is het volume van 72,0 gram zwaveldioxide?
Wat is het volume van 72,0 gram zwaveldioxide?  Onderzoekers pleiten voor beter gebruik van chemische hulpmiddelen om biomedisch onderzoek te verbeteren
Onderzoekers pleiten voor beter gebruik van chemische hulpmiddelen om biomedisch onderzoek te verbeteren Wat gebeurt er met vaste vloeistoffen of gassen wanneer ze absorberen en de hoeveelheid warmte vrijgeven?
Wat gebeurt er met vaste vloeistoffen of gassen wanneer ze absorberen en de hoeveelheid warmte vrijgeven?
 Hoeveel mensen kan onze energievoorziening ondersteunen?
Hoeveel mensen kan onze energievoorziening ondersteunen?  Vulkaanuitbarstingen verminderen wereldwijde regenval
Vulkaanuitbarstingen verminderen wereldwijde regenval Eerste resultaten van de paleomagnetische studie van Cumbre Vieja
Eerste resultaten van de paleomagnetische studie van Cumbre Vieja Crowdsourcing van vervuilingsgegevens kan de volksgezondheid ten goede komen
Crowdsourcing van vervuilingsgegevens kan de volksgezondheid ten goede komen Onderzoekers ontwikkelen stresstest om te voorspellen hoe diatomeeën zullen reageren op verzuring van de oceaan
Onderzoekers ontwikkelen stresstest om te voorspellen hoe diatomeeën zullen reageren op verzuring van de oceaan
Hoofdlijnen
- Wat is het belang van wormen?
- Wat is vergelijkbaar met chloroplasten en mitochondria?
- Hoe erfelijke ziekten werken
- Waar is Iridium een voorbeeld van?
- Indringende vraag:Wat is een neutrino?
- Wat is een dorsale wortel en wat voor soort neuron in deze structuur?
- Hoe worden de codes voor eiwitten van kern naar ribosomen gedragen?
- Wat zijn 4 kenmerken die alle soorten cellen gemeen hebben?
- Waarom Labrador retrievers meer geïnteresseerd zijn in voedsel dan andere rassen
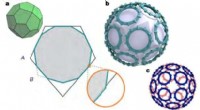
- Onderzoekers creëren onmogelijke eiwitkooien van nanoformaat met behulp van goud
- Onderzoekers ontwikkelen hulpmiddel om te helpen bij ontwikkeling, efficiëntie van auto's op waterstof

- Termietendarmmicroben kunnen de productie van biobrandstoffen ondersteunen

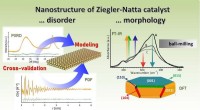
- Opheldering van nanostructuren in praktische heterogene katalysatoren
- De tijd die nodig is om de belangrijkste moleculen te sequensen, kan worden teruggebracht van jaren tot minuten
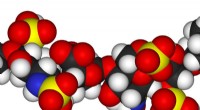
 Nieuw onderzoek beschrijft hoe uitgehongerde cellen eiwittransportstations kapen
Nieuw onderzoek beschrijft hoe uitgehongerde cellen eiwittransportstations kapen  Wat de belangrijkste sterren in Orion?
Wat de belangrijkste sterren in Orion?  Wanneer een snelheid zijn kinetische energie verdrievoudigt?
Wanneer een snelheid zijn kinetische energie verdrievoudigt?  Eerste melding van wondbehandeling door een wild dier met een pijnstillende plant
Eerste melding van wondbehandeling door een wild dier met een pijnstillende plant  Afbeelding:Hubble ziet een merkwaardige spiraal
Afbeelding:Hubble ziet een merkwaardige spiraal Hoe je jezelf kunt uiten als je wilt dat anderen met je samenwerken
Hoe je jezelf kunt uiten als je wilt dat anderen met je samenwerken Wat is een elektrisch legende -diagram?
Wat is een elektrisch legende -diagram?  Welke term hoort niet bij corpuscles Pacinian Merkel Cellen Arrector Pili?
Welke term hoort niet bij corpuscles Pacinian Merkel Cellen Arrector Pili?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

