
Wetenschap
Hoe kan een atoom worden geïoniseerd?
ionisatie door elektronen te verwijderen (positieve ionen)
* botsing met andere deeltjes: Een atoom kan worden geïoniseerd door te botsen met hoge energie-deeltjes zoals fotonen (licht), elektronen of andere atomen. Deze botsing kan voldoende energie geven om de elektrostatische aantrekkingskracht tussen de kern en een elektron te overwinnen, waardoor het elektron wordt uitgeworpen.
* Hoge temperaturen: Bij extreem hoge temperaturen bewegen de atomen snel en botsen vaker met elkaar, waardoor de kans dat een elektron wordt uitgeworpen toeneemt.
* elektrische velden: Sterke elektrische velden kunnen elektronen wegtrekken van het atoom.
ionisatie door elektronen te winnen (negatieve ionen)
* Botsing met gratis elektronen: Een atoom kan een elektron krijgen als het botst met een vrij elektron dat voldoende energie heeft om de elektrostatische afstoting tussen de bestaande elektronen van het atoom te overwinnen.
* Chemische reacties: In sommige chemische reacties kunnen atomen elektronen krijgen om negatieve ionen te vormen.
Sleutelpunten:
* ionen: Atomen die elektronen hebben gewonnen of verloren, worden ionen genoemd.
* kationen: Atomen die elektronen hebben verloren, hebben een positieve lading en worden kationen genoemd.
* anionen: Atomen die elektronen hebben gewonnen, hebben een negatieve lading en worden anionen genoemd.
Voorbeelden:
* Natrium (NA) verliest één elektron om een natriumion te vormen (Na+).
* chloor (CL) krijgt één elektron om een chloride-ion te vormen (Cl-).
Toepassingen van ionisatie:
Ionisatie heeft tal van toepassingen in wetenschap en technologie, waaronder:
* massaspectrometrie: Gebruikt om verschillende moleculen in een monster te identificeren en te kwantificeren.
* Plasma -fysica: Gebruikt om plasma's (geïoniseerde gassen) te maken en te bestuderen).
* röntgendetectoren: Gebruikt om röntgenfoto's te detecteren en te meten.
* Medische beeldvorming: Gebruikt in technieken zoals CT-scans en röntgenbeeldvorming.
 Door genetisch materiaal op te sporen, snelle sensor heeft potentieel gebruik als klinisch hulpmiddel
Door genetisch materiaal op te sporen, snelle sensor heeft potentieel gebruik als klinisch hulpmiddel Chemici ontwikkelen nieuwe methode voor selectieve binding van eiwitten
Chemici ontwikkelen nieuwe methode voor selectieve binding van eiwitten Maakt Novacaine je gas?
Maakt Novacaine je gas?  Welke metalen worden in de kern gevonden?
Welke metalen worden in de kern gevonden?  Wat is de dichtheid van gallium als aluminium een dichtheid van 2,70 gcm3 heeft en boor 2,08 gcm3?
Wat is de dichtheid van gallium als aluminium een dichtheid van 2,70 gcm3 heeft en boor 2,08 gcm3?
 Onrealistische experimenten betekenen dat de werkelijke impact van stikstofvervuiling op het milieu onbekend is
Onrealistische experimenten betekenen dat de werkelijke impact van stikstofvervuiling op het milieu onbekend is Waar zijn de twee dingen waar het klimaat uit bestaat?
Waar zijn de twee dingen waar het klimaat uit bestaat?  Positieve effecten van muskieten
Positieve effecten van muskieten Een miljoen vroegtijdige sterfgevallen als gevolg van luchtvervuiling door ozon
Een miljoen vroegtijdige sterfgevallen als gevolg van luchtvervuiling door ozon Klimaatverandering voorspellen
Klimaatverandering voorspellen
Hoofdlijnen
- Wat is soorten met blond haar en blauwe of bruine ogen?
- Welke van de volgende processen vinden plaats in de ribosomen van een cel?
- Wanneer nemen cellen hun unieke kenmerken aan?
- Wat is gist klonen?
- De moleculen die extracellulaire signalen omzetten in intracellulaire signalen zijn?
- Wat zijn de kenmerken van het leven?
- Hoe reproduceert een Yersinia -pestis zich?
- Genetische barcodes worden gebruikt om cruciale populaties in een ecosysteem van koraalriffen te kwantificeren
- Wat heeft Rosalind Franklin te maken met genetica?
- Plantaardige eiwitten uitdrogen met de snelheid van het geluid

- Kameleonmaterialen:de oorsprong van kleurvariatie in laagdimensionale perovskieten
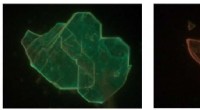
- Hi-res afbeelding van structuur van het oorsprongherkenningscomplex gebonden aan DNA onthuld
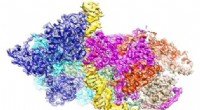
- Nieuwe methode voor de ontwikkeling van choline-acetyltransferaseremmers

- Slimme magnetische zachte materialen om kunstmatige spieren en therapeutische robots te ontwikkelen

 Wat is de meest voorkomende soort ster in de buurt van de zon?
Wat is de meest voorkomende soort ster in de buurt van de zon?  Ingenieurs ontwikkelen effectiever MRI-contrastmiddel voor kankerdetectie
Ingenieurs ontwikkelen effectiever MRI-contrastmiddel voor kankerdetectie Houdt u van uw auto? Te gehecht raken kan kostbaar zijn
Houdt u van uw auto? Te gehecht raken kan kostbaar zijn  Wat is het verschil tussen atomen en statische elektriciteit?
Wat is het verschil tussen atomen en statische elektriciteit?  Een potlood dat op een bureau rust, is een voorbeeld van wat voor soort energie?
Een potlood dat op een bureau rust, is een voorbeeld van wat voor soort energie?  Hoe wordt de vorm van een vlakke effectsnelheid?
Hoe wordt de vorm van een vlakke effectsnelheid?  Wat is de term die wordt gebruikt voor het aantal chromosomen dat in een cel wordt gevonden?
Wat is de term die wordt gebruikt voor het aantal chromosomen dat in een cel wordt gevonden?  Een geïsoleerde kei achtergelaten door een gletsjer?
Een geïsoleerde kei achtergelaten door een gletsjer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

