
Wetenschap
Wie is resultaten aangetoond dat elementen in specifieke verhoudingen worden gecombineerd omdat ze zijn gemaakt van individuele atomen?
Dalton's atomaire theorie , op basis van zijn observaties en experimenten, stelde het volgende voor:
* elementen zijn samengesteld uit kleine, ondeelbare deeltjes die atomen worden genoemd.
* atomen van hetzelfde element zijn identiek in massa en eigenschappen.
* Atomen van verschillende elementen hebben verschillende massa's en eigenschappen.
* chemische reacties omvatten de herschikking van atomen, niet hun creatie of vernietiging.
Dalton's wet van meerdere verhoudingen dit concept verder gestold. Deze wet stelt dat wanneer twee elementen meer dan één verbinding vormen, de massa's van het ene element die combineren met een vaste massa van het andere element zijn in verhoudingen van kleine hele getallen. Koolstof en zuurstof kunnen bijvoorbeeld twee verbindingen vormen:koolmonoxide (CO) en koolstofdioxide (CO₂). De verhouding van zuurstofatomen in CO tot co₂ is 1:2, die aansluit bij Dalton's theorie van atomen die in specifieke verhoudingen worden gecombineerd.
Andere belangrijke bijdragers aan de ontwikkeling van atomaire theorie zijn onder meer:
* Joseph Proust: Zijn wet van duidelijke verhoudingen verklaarde dat een gegeven chemische verbinding altijd dezelfde elementen in dezelfde verhouding bevat door massa.
* Antoine Lavoisier: Zijn werk aan het behoud van de massa hielp de basis te leggen voor de atomaire theorie van Dalton.
Hoewel de atoomtheorie van Dalton in de loop van de tijd is aangepast met de ontdekking van subatomaire deeltjes en isotopen, blijft het een fundamentele hoeksteen van de moderne chemie, wat een kader biedt voor het begrijpen van de aard van materie en chemische reacties.
 Regulering van CO2 in het lichaam
Regulering van CO2 in het lichaam Kun je trisodiumcitraat gebruiken in plaats van natrium 2 hydrateren?
Kun je trisodiumcitraat gebruiken in plaats van natrium 2 hydrateren?  Met behulp van elektriciteit vinden wetenschappers een veelbelovende nieuwe methode om chemische reacties te stimuleren
Met behulp van elektriciteit vinden wetenschappers een veelbelovende nieuwe methode om chemische reacties te stimuleren  Schrijf de volledige ionische vergelijking voor reactie die optreedt wanneer een paar druppels kaliumhydroxide -oplossing aan buffer worden toegevoegd?
Schrijf de volledige ionische vergelijking voor reactie die optreedt wanneer een paar druppels kaliumhydroxide -oplossing aan buffer worden toegevoegd?  Welke staat van materie is FESO4?
Welke staat van materie is FESO4?
 Milieuwetenschappers:tot 20% van de wereldwijde grondwaterbronnen dreigt op te drogen
Milieuwetenschappers:tot 20% van de wereldwijde grondwaterbronnen dreigt op te drogen Kun je per vakgebied natuur- en aardwetenschappen een voorbeeld geven van een functie?
Kun je per vakgebied natuur- en aardwetenschappen een voorbeeld geven van een functie?  Wat is de betekenis van fysieke gevaren?
Wat is de betekenis van fysieke gevaren?  Droogte treft rivier Zuid-Amerika, een enorm ecosysteem bedreigend
Droogte treft rivier Zuid-Amerika, een enorm ecosysteem bedreigend Stedelijke groei, hitte eilanden, vochtigheid, klimaatverandering:kosten vermenigvuldigen in tropische steden
Stedelijke groei, hitte eilanden, vochtigheid, klimaatverandering:kosten vermenigvuldigen in tropische steden
Hoofdlijnen
- Hoe wordt microscoop gebruikt om informatie te verzamelen?
- Welke basis is niet aanwezig in de nucleotiden van RNA?
- Wat zijn twee typen endoplasmatisch reticulum?
- Vermijd sommige hondenoogdoekjes van Project Watson vanwege infectiegevaar, waarschuwt de consumentencommissie
- Welke kenmerken van de bladeren helpen het meeste voedsel te maken door fotosynthese?
- Op welke manieren zijn de bloemen vergelijkbaar met het reproductieve systeem van dieren?
- Waarom moet een organisme stabiele interne omstandigheden handhaven?
- Welke delen van de cel zijn betrokken bij cellulaire ademhaling?
- Wat zijn de overeenkomsten tussen studie van wetenschap en literatuur?
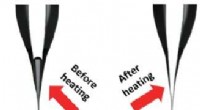
- Volledige vulling van batches nanopipetten
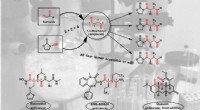
- Wanneer zwavel spoorloos verdwijnt
- Computermodel voor het ontwerpen van eiwitsequenties die zijn geoptimaliseerd om te binden aan medicijndoelen

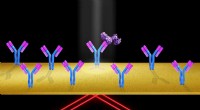
- Techniek maakt handig, nauwkeurige optische beeldvorming van individuele eiwitten
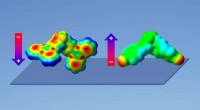
- Kleine moleculen, gigantisch (oppervlakte)potentieel
 Best case-doelen voor klimaatopwarming die nog steeds kunnen resulteren in een enorm natuurbrandrisico
Best case-doelen voor klimaatopwarming die nog steeds kunnen resulteren in een enorm natuurbrandrisico Welke soorten materialen zijn slechte geleiders warmte?
Welke soorten materialen zijn slechte geleiders warmte?  Celtoxinen nader bekeken:Onderzoekers onderzoeken hoe radionucliden interageren met niercellen
Celtoxinen nader bekeken:Onderzoekers onderzoeken hoe radionucliden interageren met niercellen  Onderscheid maken tussen negatieve exponentiële punten
Onderscheid maken tussen negatieve exponentiële punten Wat is de beweging van een medium?
Wat is de beweging van een medium?  Chemici maken playdough / Lego-achtige hybride om kleine bouwstenen te maken
Chemici maken playdough / Lego-achtige hybride om kleine bouwstenen te maken Wat zijn de belangrijkste twee nadelen van zonne -energie?
Wat zijn de belangrijkste twee nadelen van zonne -energie?  Wat is bi2SbTe3?
Wat is bi2SbTe3?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

