
Wetenschap
Met behulp van elektriciteit vinden wetenschappers een veelbelovende nieuwe methode om chemische reacties te stimuleren
Nu de wereld zich afwendt van gas naar elektriciteit als groenere energiebron, gaat de to-do-lijst verder dan alleen auto’s. Het enorme wereldwijde productienetwerk dat alles maakt, van onze batterijen tot onze meststoffen, moet ook de schakelaar omzetten.
Een onderzoek van scheikundigen van UChicago heeft een manier gevonden om elektriciteit te gebruiken om een soort chemische reactie te stimuleren die vaak wordt gebruikt bij het synthetiseren van nieuwe kandidaten voor farmaceutische medicijnen.
Gepubliceerd op 2 januari in Natuurkatalyse , is het onderzoek een vooruitgang op het gebied van de elektrochemie en toont het een weg voorwaarts in het ontwerpen en controleren van reacties – en het duurzamer maken ervan.
"Wat we willen doen is begrijpen wat er op het fundamentele niveau van de elektrode-interface gebeurt, en dat gebruiken om efficiëntere chemische reacties te voorspellen en te ontwerpen", zegt Anna Wuttig, UChicago Neubauer Family Assistant Professor en senior auteur van het artikel. "Dit is een stap in de richting van dat uiteindelijke doel."
Chemische complexiteit
Bij bepaalde chemische reacties kan elektriciteit de opbrengst verhogen – en omdat je de benodigde elektriciteit uit hernieuwbare bronnen kunt halen, kan dit deel uitmaken van het groener maken van de wereldwijde chemische industrie.
Maar de elektrochemie, zoals het vakgebied bekend staat, is bijzonder complex. Er is veel dat wetenschappers niet weten over de moleculaire interacties, vooral omdat je een geleidende vaste stof (een elektrode) in het mengsel moet steken om de elektriciteit te leveren, wat betekent dat de moleculen zowel met die elektrode als met elkaar interageren. Voor een wetenschapper die probeert de rollen te ontwarren die elk molecuul speelt en in welke volgorde, maakt dit een toch al ingewikkeld proces nog ingewikkelder.
Wuttig wil hier echter een voordeel van maken. "Wat als je het beschouwt als elektrochemie die ons een unieke ontwerphefboom biedt die in geen enkel ander systeem mogelijk is?" zei ze.
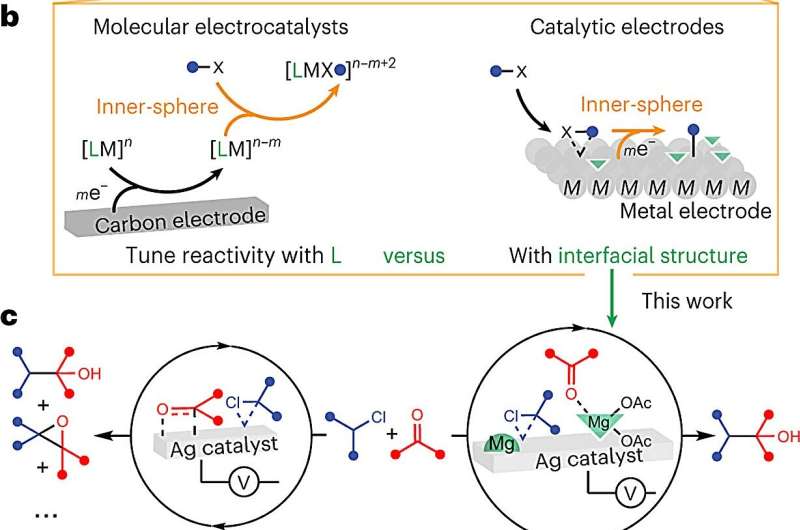
In dit geval concentreerden zij en haar team zich op het oppervlak van de elektrode die de elektriciteit voor de reactie levert.
"Er waren aanwijzingen dat het oppervlak zelf katalytisch is, dat het een rol speelt," zei Wuttig, "maar we weten niet hoe we die interacties op moleculair niveau systematisch moeten controleren."
Ze sleutelden aan een soort reactie die vaak wordt gebruikt bij de productie van chemicaliën voor medicijnen, om een binding tussen twee koolstofatomen te vormen.
Volgens theoretische voorspellingen zou de opbrengst van de reactie 100% moeten zijn, wanneer deze reactie wordt uitgevoerd met behulp van elektriciteit. Dat wil zeggen dat van alle moleculen die erin zijn gegaan, een enkele nieuwe substantie is gemaakt. Maar als je de reactie daadwerkelijk in het laboratorium uitvoert, is de opbrengst lager.
Het team dacht dat de aanwezigheid van de elektrode sommige moleculen wegleidde van waar ze nodig waren tijdens de reactie. Ze ontdekten dat het toevoegen van een belangrijk ingrediënt zou kunnen helpen:een chemische stof die bekend staat als een Lewis-zuur, toegevoegd aan de vloeibare oplossing, leidde die moleculen om.
"Je krijgt een vrijwel zuivere reactie", zei Wuttig.
Verandering katalyseren
Bovendien kon het team speciale beeldvormingstechnieken gebruiken om de reacties op moleculair niveau te volgen. "Je kunt zien dat de aanwezigheid van de modulator een diepgaand effect heeft op de grensvlakstructuur", zei ze. "Hierdoor kunnen we visualiseren en begrijpen wat er gebeurt, in plaats van het als een zwarte doos te beschouwen."
Dit is een cruciale stap, zegt Wuttig, omdat het een weg vooruit laat zien naar het niet alleen kunnen gebruiken van de elektrode in de chemie, maar ook naar het voorspellen en controleren van de effecten ervan.
Een ander voordeel is dat de elektrode voor meer reacties kan worden hergebruikt. (Bij de meeste reacties wordt de katalysator opgelost in de vloeistof en tijdens het zuiveringsproces afgevoerd om het eindproduct te verkrijgen).
"Dit is een stap in de richting van duurzame synthese", zei ze. "In de toekomst is mijn groep erg enthousiast om dit soort concepten en strategieën te gebruiken om andere synthetische uitdagingen in kaart te brengen en aan te pakken."
Meer informatie: Qiu-Cheng Chen et al., Grensvlakafstemming van elektrokatalytische Ag-oppervlakken voor fragmentgebaseerde elektrofiele koppeling, Natuurkatalyse (2024). DOI:10.1038/s41929-023-01073-5
Journaalinformatie: Natuurkatalyse
Aangeboden door Universiteit van Chicago
 Katalysator gemaakt van ijzer kan een belangrijke reactie veroorzaken voor het maken van organische verbindingen
Katalysator gemaakt van ijzer kan een belangrijke reactie veroorzaken voor het maken van organische verbindingen Risico's van ademhalingsolie Smoke
Risico's van ademhalingsolie Smoke De kans op succes in de synthetische chemie vergroten
De kans op succes in de synthetische chemie vergroten Het gebruik van reinigingstechnologieën optimaliseren
Het gebruik van reinigingstechnologieën optimaliseren Chemische reacties visualiseren met infraroodthermografie
Chemische reacties visualiseren met infraroodthermografie
 De vervuilingsregels van Trump worden teruggedraaid om steenkoolland hard te raken
De vervuilingsregels van Trump worden teruggedraaid om steenkoolland hard te raken Recycling van plastic flessen Carbios haalt donateurs op
Recycling van plastic flessen Carbios haalt donateurs op Voor zombiemicroben, diepzeebuffet is net buiten bereik
Voor zombiemicroben, diepzeebuffet is net buiten bereik Gemeenschappelijke huishoudelijke verontreinigende stoffen
Gemeenschappelijke huishoudelijke verontreinigende stoffen  Studie volgt de adoptie van groene infrastructuur, van waterbesparing tot beleid
Studie volgt de adoptie van groene infrastructuur, van waterbesparing tot beleid
Hoofdlijnen
- Californië verbiedt de zalmvisserij voor het seizoen in de rivieren in het Sacramento-gebied en het Klamath-bekken
- Vier nieuwe soorten slakken beschreven
- Onderzoekers ontrafelen de kristalstructuur van een belangrijk enzym van SARS-CoV-2, wat de weg vrijmaakt voor nieuwe antivirale middelen
- Woestijn in Zuid-Californië overspoeld met de beste superbloei in 20 jaar
- Dolfijnen gebruiken kenmerkende fluitjes om andere dolfijnen te vertegenwoordigen, vergelijkbaar met hoe mensen namen gebruiken
- Wetenschappers controleren cellen met licht,
- Kunnen darmbacteriën de volgende sportdrank worden?
- Het chocoladeaanbod ter wereld wordt bedreigd door een verwoestend virus
- Onderzoekers onthullen nieuwe inzichten in de controle van cellulaire steigers
- AI-agent helpt materiaaleigenschappen sneller te identificeren

- Nieuwe manier om taaie koolstofbindingen te splitsen kan deuren openen voor groenere chemicaliën

- De mechanismen van verbeterde verdampingsflux door nanokanalen

- Wetenschappers maken kunstmatige katalysatoren geïnspireerd door levende enzymen

- Onderzoekers zetten AI aan het werk bij het maken van scheikundige voorspellingen

 Experts ontwikkelen nieuw mechanisme dat submicrondeeltjes in minuten kan vangen
Experts ontwikkelen nieuw mechanisme dat submicrondeeltjes in minuten kan vangen Onderzoekers synthetiseren een nanocluster van supergefluoreerd goud
Onderzoekers synthetiseren een nanocluster van supergefluoreerd goud Ingenieurs ontwikkelen nieuwe manier om de intentie van leugenaars te kennen
Ingenieurs ontwikkelen nieuwe manier om de intentie van leugenaars te kennen 'S Werelds breedste grafeen nanoribbon belooft de volgende generatie geminiaturiseerde elektronica
'S Werelds breedste grafeen nanoribbon belooft de volgende generatie geminiaturiseerde elektronica Een nieuw idee voor het snel genereren van sterke magnetische velden met behulp van laserpulsen
Een nieuw idee voor het snel genereren van sterke magnetische velden met behulp van laserpulsen Onderzoekers vinden bewijs voor metallische waterstof bij 425 gigapascal
Onderzoekers vinden bewijs voor metallische waterstof bij 425 gigapascal Een bemanning van 500 in leven houden voor de reis naar een andere ster
Een bemanning van 500 in leven houden voor de reis naar een andere ster Koolstofgasopslagcaverne is de beste manier om schone energie uit een fossiele brandstof te halen
Koolstofgasopslagcaverne is de beste manier om schone energie uit een fossiele brandstof te halen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

