
Wetenschap
Behouden gassen hetzelfde volume?
* gassen zijn samendrukbaar: In tegenstelling tot vaste stoffen en vloeistoffen hebben gassen zeer zwakke intermoleculaire krachten. Dit betekent dat hun moleculen ver uit elkaar liggen en dichter bij elkaar kunnen worden geperst.
* Volume hangt af van druk en temperatuur: Het volume van een gas is direct gerelateerd aan de druk en temperatuur waaraan het wordt blootgesteld.
* Druk: Het verhogen van de druk op een gas dwingt de moleculen dichter bij elkaar, waardoor het volume wordt verlaagd.
* Temperatuur: Het verhogen van de temperatuur van een gas geeft de moleculen meer kinetische energie, waardoor ze sneller bewegen en zich verspreiden, waardoor het volume wordt verhoogd.
Voorbeeld: Denk aan een ballon. Wanneer u er lucht in blaast, verhoogt u de druk erin. De gasmoleculen worden dichterbij geperst, waardoor de druk wordt verhoogd totdat de ballon uitzet.
Key Takeaway: Het volume van een gas is niet vast en kan veranderen, afhankelijk van de omstandigheden waarin het zich bevindt.
 Waarom staten doorgaan met schone energie ondanks Trumps omhelzing van steenkool?
Waarom staten doorgaan met schone energie ondanks Trumps omhelzing van steenkool? Wat kunnen we leren van computationele archeologie?
Wat kunnen we leren van computationele archeologie?  NASA wordt in de gaten gehouden door grote orkaan Jose
NASA wordt in de gaten gehouden door grote orkaan Jose Het gebruik van de Eye
Het gebruik van de Eye Onderzoek naar de luchtkwaliteit binnenshuis toont aan dat vliegtuigen tijdens de vlucht de laagste deeltjesniveaus kunnen hebben
Onderzoek naar de luchtkwaliteit binnenshuis toont aan dat vliegtuigen tijdens de vlucht de laagste deeltjesniveaus kunnen hebben
Hoofdlijnen
- De diversiteit aan gewassen ter wereld documenteren en beschikbaar maken
- Wanneer het lichaam op zijn eigen cellen reageert als vreemde antigenen, resulteert dit in?
- Onderzoekers creëren een nauwkeuriger model van hoe sommige microben naar voedingsstoffen zoeken
- DNA-replicatie vergelijken en contrasteren in prokaryoten en eukaryoten
- Onderzoek bevestigt dat identiteitsverwisseling kan verklaren waarom haaien mensen bijten
- Welke factoren beïnvloeden de werking van enzymen en waarom?
- Een dam gebouwd in de Amazone creëerde duizenden boseilanden, maar ze zijn te klein om de meeste soorten in stand te houden
- Waarom zeevarende zoogdieren groter moeten zijn dan landrotten
- Wat is een biomechanische analyse?
- Synthetisch rubber presteert beter dan natuurlijk rubber

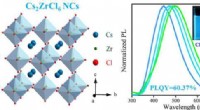
- Wetenschappers synthetiseren loodvrije op zirkonium gebaseerde vacature-geordende dubbele perovskiet nanokristallen
- Monstervoorbereiding in forensische toxicologische analyse kan enorme gevolgen hebben

- Forensisch chemicus detecteert marihuanagebruik op basis van zweettest

- Peptide-hydrogels kunnen traumatisch hersenletsel helpen genezen

 Studie stelt slimme hechtingen voor met sensoren voor wonden
Studie stelt slimme hechtingen voor met sensoren voor wonden In welke organel komt fotosynthese en cellulaire ademhaling op?
In welke organel komt fotosynthese en cellulaire ademhaling op?  Vormen 0,1 mol HCl en 0,2 NaOH een buffer?
Vormen 0,1 mol HCl en 0,2 NaOH een buffer?  Welk volume oplosmiddel moet worden toegevoegd aan 36,8 g CH3OH om een 0,500 M oplossing CH3OH te verkrijgen?
Welk volume oplosmiddel moet worden toegevoegd aan 36,8 g CH3OH om een 0,500 M oplossing CH3OH te verkrijgen?  Wat betekent in de wetenschap?
Wat betekent in de wetenschap?  Waar is een object dat stationair is ten opzichte van het aardoppervlak dat de snelste ruimte beweegt?
Waar is een object dat stationair is ten opzichte van het aardoppervlak dat de snelste ruimte beweegt?  Een simulatie van het stempelen van metalen platen belooft een verbeterde productie van auto-onderdelen
Een simulatie van het stempelen van metalen platen belooft een verbeterde productie van auto-onderdelen Elektriciteit opgewekt met water, zout en een membraan van drie atomen dik
Elektriciteit opgewekt met water, zout en een membraan van drie atomen dik
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

