
Wetenschap
Wat is er in een nat type volt -voltic -cel elektrolyt?
Hier is een uitsplitsing:
* elektrolyt: Het hart van de natte cel, het biedt het medium voor de beweging van ionen.
* ionen: Geladen deeltjes (atomen of moleculen) die verantwoordelijk zijn voor het dragen van de elektrische stroom.
* elektroden: De vaste geleiders die deelnemen aan de chemische reacties en waar de elektrische stroom wordt gegenereerd.
Waarom is de elektrolyt belangrijk?
* Vergemakkelijkt ionisch transport: Met de elektrolyt kunnen ionen tussen de elektroden bewegen, het circuit voltooien en een elektrische stroom genereren.
* handhaaft ladingsbalans: Terwijl de chemische reacties optreden, helpt de elektrolyt de elektrische neutraliteit van de cel te behouden door ionen te leveren om de ladingen die zich op de elektroden ophopen te neutraliseren.
Voorbeelden van elektrolyten in natte cellen:
* Verdun zwavelzuur: Vaak gebruikt in loodzuurbatterijen.
* kaliumhydroxide: Gebruikt in alkalische batterijen.
* ammoniumchloride: Gebruikt in sommige soorten droge cellen.
Sleutelpunt: De gebruikte specifieke elektrolyt hangt af van het type natte cel en de chemische reacties die erin plaatsvinden.
Hoofdlijnen
- Hoe zorgden dinosaurussen voor botverpletterende beten? Door een stijve onderkaak te houden.
- Nieuwe aanpak kan de sleutel zijn tot de behandeling van antibioticaresistente bacteriën
- Planten kunnen zichzelf verdedigen door rupsen kannibaal te maken
- Waarom zijn de roze meren van Australië roze?
- Welke planten maken medicijnen?
- Ontdekt in planten een mechanisme dat defecten in eiwitvouwing corrigeert
- Wanneer gaan organismen door het mitoseproces?
- Kan ik een medicijn nemen om een bepaalde herinnering uit te wissen?
- Het diploïde getal bij paarden is 64. Wat is het haploïde van de chromosomen van paarden?
- Beheersing van ijsvorming op gradiëntbevochtigbare oppervlakken voor hoogwaardige bio-geïnspireerde materialen

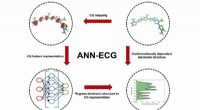
- Nieuwe benadering van moleculaire modellering kan de ontwikkeling van nieuwe organische materialen voor elektronica versnellen
- Lifters belemmeren de houdbaarheid van medicijnen

- De genen vinden om een betere kankerbehandeling op te bouwen

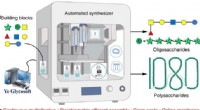
- Geautomatiseerde koolhydraatsynthesizer produceert polysachariden met een recordlengte
 De innerlijke geheimen van nanodraden onderzoeken
De innerlijke geheimen van nanodraden onderzoeken Hoe wordt het genoemd als een organisme genen heeft die anders zijn voor een eigenschap?
Hoe wordt het genoemd als een organisme genen heeft die anders zijn voor een eigenschap?  Een 3D-aanpak om kanker te stoppen
Een 3D-aanpak om kanker te stoppen Overschilderbare elektronica? Wetenschappers bestuderen spray-on-productie van transistors
Overschilderbare elektronica? Wetenschappers bestuderen spray-on-productie van transistors  Europese zeebaars absorbeert vrijwel geen microplastic in hun spierweefsel
Europese zeebaars absorbeert vrijwel geen microplastic in hun spierweefsel Nieuwe klasse van crosslinker-vrije biomaterialen van nanovezels van Hydra-nematocyst-eiwitten
Nieuwe klasse van crosslinker-vrije biomaterialen van nanovezels van Hydra-nematocyst-eiwitten Licht zou halfgeleidercomputers een miljoen keer sneller kunnen maken of zelfs kwantum kunnen maken
Licht zou halfgeleidercomputers een miljoen keer sneller kunnen maken of zelfs kwantum kunnen maken Hoe verhoudt cirkelvormige beweging zich tot de wetten van Newton?
Hoe verhoudt cirkelvormige beweging zich tot de wetten van Newton?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


