
Wetenschap
Wat is de reactie tussen zuren en basen?
Wat gebeurt er:
* zuur (Typisch bevattende waterstofionen, H+) reageert met een basis (meestal met hydroxide-ionen, oh-) om zout te vormen en water .
* De waterstofionen van het zuur combineren met de hydroxide -ionen van de basis om water te vormen (H2O).
* De resterende ionen van het zuur en de basis combineren om een zout te vormen.
Algemene vergelijking:
Zuur + base → zout + water
Voorbeeld:
* zoutzuur (HCl) + natriumhydroxide (NaOH) → natriumchloride (NaCl) + water (H2O)
Sleutelpunten:
* neutralisatie is een exotherme reactie , wat betekent dat het warmte vrijgeeft.
* De pH van de oplossing verandert. Zure oplossingen hebben een pH minder dan 7, terwijl basisoplossingen een pH groter dan 7 hebben. Neutralisatie brengt de pH dichter bij 7.
* De sterkte van het zuur en de basis bepaalt de mate van de reactie. Sterkere zuren en basen reageren krachtiger.
Toepassingen:
Neutralisatiereacties hebben talloze toepassingen, waaronder:
* het beheersen van de zuurgraad in industriële processen
* Digestie in ons lichaam (maagzuur wordt geneutraliseerd door bicarbonaationen)
* Salt produceren (veel zouten worden geproduceerd door neutralisatiereacties)
* Antacida maken (om overtollig maagzuur te neutraliseren)
Laat het me weten als je nog meer vragen hebt!
 Mechanismemodellering voor betere voorspellingen, klimaatvoorspellingen
Mechanismemodellering voor betere voorspellingen, klimaatvoorspellingen Terugkeer van ondergedoken watervegetatie is de schildwacht van het ecosysteemherstel van Chesapeake Bay
Terugkeer van ondergedoken watervegetatie is de schildwacht van het ecosysteemherstel van Chesapeake Bay Is de wasachtige laag van een blad dikker dan de epidermis?
Is de wasachtige laag van een blad dikker dan de epidermis?  Wijdverbreide ineenstorting van de ijskap van West-Antarctica is te vermijden als we de opwarming van de aarde onder de 2 graden houden
Wijdverbreide ineenstorting van de ijskap van West-Antarctica is te vermijden als we de opwarming van de aarde onder de 2 graden houden Nieuwe, op GPS gebaseerde methode kan het dagelijkse ijsverlies in Groenland meten
Nieuwe, op GPS gebaseerde methode kan het dagelijkse ijsverlies in Groenland meten
Hoofdlijnen
- Wat zijn dochtercellen geproduceerd wanneer ze mitose ondergaan, genetisch zijn?
- Wat zijn feiten die de evolutie weerleggen?
- Zijn microtubuli gevonden in dier- of plantencellen?
- Inzicht in cellulaire transcriptiereacties op zuurstofgebrek
- Waarom evolueerden mensen maar wangen?
- Waarom de harde Sneeuwbalaarde onze vroegste meercellige voorouders op gang bracht
- Welke organel bevat chlorofyl en is de locatie voor fotosynthese?
- Wat is eigenlijk haploïde?
- Veel dingen kunnen er een creëren.
- Pharma streeft naar een betere CBD

- Nieuwe bio-geïnspireerde lijm hecht elk oppervlak onder water

- Minder energie nodig om CO2-afval om te zetten in waardevolle hulpbronnen

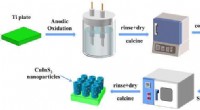
- CuInS2/TiO2-fotoanodecomposieten presteren goed in fotogeïnduceerde kathodische bescherming
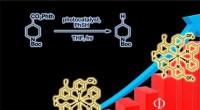
- Geïnspireerd door fotosynthese, wetenschappers dubbele reactie kwantumefficiëntie
 Deskundigen stellen een langetermijnstrategie voor voor het risicobeheer van natuurbranden in het tijdperk van klimaatverandering
Deskundigen stellen een langetermijnstrategie voor voor het risicobeheer van natuurbranden in het tijdperk van klimaatverandering  Wie heeft geprobeerd de relatieve afstanden te meten Maan en zon?
Wie heeft geprobeerd de relatieve afstanden te meten Maan en zon?  Van rare PhD-sterrenkijker tot Nobelprijswinnaar Natuurkunde
Van rare PhD-sterrenkijker tot Nobelprijswinnaar Natuurkunde First things first:om de klimaatdoelstellingen te halen, we kunnen de lagere stappen van de mitigatiehiërarchie niet overslaan
First things first:om de klimaatdoelstellingen te halen, we kunnen de lagere stappen van de mitigatiehiërarchie niet overslaan Wat voor soort regio is het waar verschillende universiteiten zijn?
Wat voor soort regio is het waar verschillende universiteiten zijn?  Verbrandt een sterrengas anders dan helium en waterstof als dat zo is, welke gassen kleur maken ze de ster?
Verbrandt een sterrengas anders dan helium en waterstof als dat zo is, welke gassen kleur maken ze de ster?  Franse vakbonden speelden een sleutelrol bij de bescherming van de geestelijke gezondheid van werknemers
Franse vakbonden speelden een sleutelrol bij de bescherming van de geestelijke gezondheid van werknemers Wat voor soort cel wordt gevormd als chromosomen van een sperma -oproep en een eiermoeken?
Wat voor soort cel wordt gevormd als chromosomen van een sperma -oproep en een eiermoeken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

