
Wetenschap
Wat zijn de meest reactieve niet -metalen in halogenen?
Dit is waarom:
* elektronegativiteit: Fluor heeft de hoogste elektronegativiteit van alle elementen, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen. Dit maakt het zeer reactief, enthousiast om een elektron te krijgen om zijn octet te voltooien. Chloor, hoewel niet zo elektronegatief als fluor, is nog steeds erg reactief.
* Elektronenaffiniteit: Fluorine heeft ook de hoogste elektronenaffiniteit, wat betekent dat het de meeste energie vrijgeeft wanneer het een elektron krijgt. Dit draagt verder bij aan zijn hoge reactiviteit.
* kleiner formaat: Fluor en chloor zijn relatief kleine atomen, wat betekent dat hun buitenste elektronen dichter bij de kern zijn en een sterkere elektrostatische aantrekkingskracht ervaren. Hierdoor reageren ze eerder om te reageren.
reactiviteitstrend binnen halogenen:
De reactiviteit van halogenen neemt af als je de groep af gaat:
* f> CL> Br> i> bij
Dit komt omdat de grotere atomen hun buitenste elektronen verder van de kern hebben, waardoor ze minder aangetrokken worden tot extra elektronen.
Laat het me weten als je nog andere vragen hebt!
 Wetenschappers ontwikkelen met maleïnezuur behandelde bacteriële cellulosegel voor het verbeteren van botherstel
Wetenschappers ontwikkelen met maleïnezuur behandelde bacteriële cellulosegel voor het verbeteren van botherstel  Wat gebeurde er met waterdamp toen de aarde zich vormde en afkoelde?
Wat gebeurde er met waterdamp toen de aarde zich vormde en afkoelde?  Hoe vind je de zuiverheid van ijzer en niet-aluin?
Hoe vind je de zuiverheid van ijzer en niet-aluin?  Met moleculaire gegevensopslag, kattenvideo's kunnen ons allemaal overleven
Met moleculaire gegevensopslag, kattenvideo's kunnen ons allemaal overleven Is het waar dat de wet van behoudsmassa -toestanden in een chemische reactie -materie kan worden gecreëerd of vernietigd?
Is het waar dat de wet van behoudsmassa -toestanden in een chemische reactie -materie kan worden gecreëerd of vernietigd?
Hoofdlijnen
- Wat gebeurt er als te veel water in een cel zit?
- Wat is het bewijs voor evolutie van niet -levende dingen?
- Wat zijn de producten en reactanten van cellulaire ademhaling waar komt het voor?
- Drone-foto's bieden snellere, goedkopere gegevens over de belangrijkste Antarctische soorten
- Welke weefseltypen blijven tijdens het leven zeer mitotisch en waarom?
- Xist- en lapjeskatten:hoe extra genen op X-chromosomen worden uitgeschakeld
- Waarom is transpiratie belangrijk in de watercyclus?
- Hoe slaaplabs werken
- Wat maakt evolutie een therory?
- Door goedkope en veilige zwart-witte materialen te combineren, ontstaan kleurrijke pigmenten

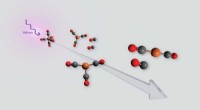
- Kijken naar licht dat een model fotokatalysator bijna in realtime afbreekt
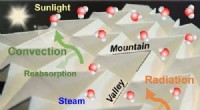
- Origami inspireert zeer efficiënte zonne-stoomgenerator
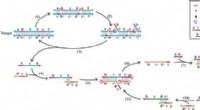
- Eenvoudig kopiëren:een universele isotherme DNA-amplificatiemethode
- Water beïnvloedt de plakkerigheid van hyaluronan

 Wat is een beschrijving van de stappen in wetenschappelijke methode-?
Wat is een beschrijving van de stappen in wetenschappelijke methode-?  Hoe interageert een Amerikaanse Robin met andere organismen in het milieu?
Hoe interageert een Amerikaanse Robin met andere organismen in het milieu?  Twee kolven van gelijke grootte zijn verbonden met één molecuul. Wat is de kans dat dat in fles A zit? Wat is het B?
Twee kolven van gelijke grootte zijn verbonden met één molecuul. Wat is de kans dat dat in fles A zit? Wat is het B?  Hebben schimmel water en zonneschijn nodig om te groeien?
Hebben schimmel water en zonneschijn nodig om te groeien?  Wat is de rol van een geoloog in de aardolie -industrie?
Wat is de rol van een geoloog in de aardolie -industrie?  Een lavastroom is een voorbeeld van stollingsrots, een van de twee hoofdgroepen?
Een lavastroom is een voorbeeld van stollingsrots, een van de twee hoofdgroepen?  Large Lot-programma toont de kracht van particulier grondbeheer bij het aanpakken van stedelijke leegstand
Large Lot-programma toont de kracht van particulier grondbeheer bij het aanpakken van stedelijke leegstand Hoe een wetenschapper het aanbevelingsalgoritme heeft toegepast om te anticiperen op de aankomsttijden van CME's
Hoe een wetenschapper het aanbevelingsalgoritme heeft toegepast om te anticiperen op de aankomsttijden van CME's
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

