
Wetenschap
Chloride oplosbaar of onoplosbaar in water?
chloride-ionen (Cl-) zijn oplosbaar in water.
Dit is waarom:
* ionische verbindingen: Chloride -ionen worden meestal aangetroffen in ionische verbindingen, waarbij ze banden vormen met positief geladen ionen (kationen).
* polariteit: Water is een polair molecuul, wat betekent dat het een enigszins positief uiteinde en een enigszins negatief uiteinde heeft.
* Attractie: Het positieve uiteinde van watermoleculen wordt aangetrokken door de negatief geladen chloride -ionen, en deze aantrekkingskracht helpt de ionische verbinding op te lossen.
Het is echter belangrijk om te onthouden dat de oplosbaarheid van een verbinding die chloride -ionen bevat, afhankelijk kan zijn van het specifieke kation waarmee het gepaard gaat.
* Oplosbare chloriden: Veel chloriden zijn oplosbaar in water, zoals natriumchloride (NaCl), kaliumchloride (KCL) en calciumchloride (CACL2).
* onoplosbare chloriden: Sommige chloriden zijn onoplosbaar of slechts enigszins oplosbaar, zoals zilverchloride (AGCL) en loodchloride (PBCL2).
Laat het me weten als je nog andere vragen hebt!
 Wat zijn de sterke en zwakke punten voor uraniumeigenschappen?
Wat zijn de sterke en zwakke punten voor uraniumeigenschappen?  Licht gebruiken om de reikwijdte van carbonyleringsreacties uit te breiden
Licht gebruiken om de reikwijdte van carbonyleringsreacties uit te breiden Is magnesiumsulfide een ionische of covalente verbinding?
Is magnesiumsulfide een ionische of covalente verbinding?  Welke ontdekking leidde J.J Thomson om te beslissen dat atomen niet onverminderd waren maar eigenlijk uit kleinere delen zijn samengesteld?
Welke ontdekking leidde J.J Thomson om te beslissen dat atomen niet onverminderd waren maar eigenlijk uit kleinere delen zijn samengesteld?  Hoeveel buitenringelektronen heeft een natriumatoom?
Hoeveel buitenringelektronen heeft een natriumatoom?
 Wat zijn de factoren die het weer en het klimaat beïnvloeden?
Wat zijn de factoren die het weer en het klimaat beïnvloeden?  Klimaatverandering kan leiden tot grotere algenbloei
Klimaatverandering kan leiden tot grotere algenbloei Satelliet toont post-tropische cycloon Selma verdwijnen
Satelliet toont post-tropische cycloon Selma verdwijnen Stormen verwoesten rijstvelden in de gouden driehoek van Italië
Stormen verwoesten rijstvelden in de gouden driehoek van Italië Webtool gemaakt door onderzoekers helpt klimaatverandering in de landbouw te voorspellen
Webtool gemaakt door onderzoekers helpt klimaatverandering in de landbouw te voorspellen
Hoofdlijnen
- Waar staan de letters voor in DNA?
- Wat zijn de vijf accessoire organen van het gastro -intestinale systeem?
- Welk type weefsel zijn de belangrijkste functiecellen dit om te verkorten?
- Wat zijn de functionele groepen van tristearine?
- Kunstmatige intelligentie helpt wetenschappers planten te ontwikkelen om de klimaatverandering te bestrijden
- Kan een kunstneus voedselbederf detecteren?
- Onderzoekers ontwikkelen een genoom op bijna chromosoomniveau voor de Mojave-papaverbij
- Wat is de naam voor een groep cellen die samenwerkt om een bepaalde taak uit te voeren in het N -organisme?
- Wat zijn de 4 hoofdonderdelen van een virus?
- Levende elektroden met bacteriën en organische elektronica

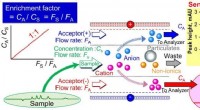
- Verbetering van de gevoeligheid voor analyse van ionische opgeloste stoffen
- Een onderzoek naar de instabiliteit van het rozenvenster

- Het uitlaatgas van een elektriciteitscentrale kan worden teruggewonnen en gebruikt als grondstof voor reactie

- Snel, nauwkeurige manier om pindaplanten te controleren op gezonde eigenschappen

 Onderzoeksteam ontwikkelt gewrichtsspalken voor sport en geneeskunde, geïnspireerd op libellenvleugels
Onderzoeksteam ontwikkelt gewrichtsspalken voor sport en geneeskunde, geïnspireerd op libellenvleugels Welke theorie is de basis van uw begrip Waardoor een magneet werkt?
Welke theorie is de basis van uw begrip Waardoor een magneet werkt?  Wanneer opgeslagen energie wordt gebruikt, is het veranderd in wat voor soort energie?
Wanneer opgeslagen energie wordt gebruikt, is het veranderd in wat voor soort energie?  Wat gebeurt er als zink in verdund zoutzuur wordt gedaan?
Wat gebeurt er als zink in verdund zoutzuur wordt gedaan?  Welk verschil maakt het voor energiebehoeften als ze zware werken doen?
Welk verschil maakt het voor energiebehoeften als ze zware werken doen?  Relatie tussen wolkenbedekking en de hoeveelheid energie die de aarde raakt?
Relatie tussen wolkenbedekking en de hoeveelheid energie die de aarde raakt?  Wat zijn de bijproducten van verzepingsvetten en -oliën?
Wat zijn de bijproducten van verzepingsvetten en -oliën?  Wanneer een meisje bovenaan haar jump -mechanische energie staat in welke vorm?
Wanneer een meisje bovenaan haar jump -mechanische energie staat in welke vorm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

